
����Ŀ��̼��ﮣ���Է�������74���㷺Ӧ���ڻ�����ұ�����ҵ����ҵ������﮻�ʯ��Li2Al2Si4Ox���Ʊ�̼��﮵�������ͼ�� 
��֪��̼��﮵��ܽ��Ϊ����g/L��
�¶� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
��ش��������⣺
��1��﮻ԣ�Li2Al2Si4Ox�����������������ʽ��ʾ����ɣ���ʽΪ
��2�����ữ�����¶ȿ�����250�橁300��֮�䣬��Ҫԭ���� �� �����������������������������l15%���ң�����������ĸ������� ��
��3��ˮ��ʱ������CaCO3��ĩ��ַ�Ӧ����ˣ���������Ҫ�ɷֳ�CaCO3��� ��
��4������ﮡ��Ļ�ѧ��Ӧ����ʽΪ ��
��5������ﮡ���Ҫ��95�����Ͻ��У���ˣԭ���� �� ����̼�������ĸҺ����Ҫ���������ƣ������ܺ����� ��
���𰸡�
��1��Li2O?Al2O3?4SiO2
��2���¶ȵ���250�棬��Ӧ���ʽ������¶ȸ���300�棬����ӷ��϶ࣻ�����л���Ҫ��ȥ���������ᣬ���Ӻ������ʵĴ����������Ӻ����к���ĸ���
��3��CaSO4��SiO2��Al��OH��3
��4��Na2CO3+Li2SO4=Li2CO3��+Na2SO4
��5���¶�Խ�ߣ�̼����ܽ�Ƚ��ͣ��������Ӳ��ʣ�̼���ƣ�̼���
���������⣺��1����1��﮻�ʯ��Li2Al2Si4Ox�����������������ʽ��ʾ��LiԪ�ػ��ϼ�+1�ۣ���Ԫ��+3�ۣ���Ԫ�ة�2�ۣ���Ԫ��+4�ۣ����ݻ��ϼ۴�����Ϊ0������ȷ��Li2Al2Si4Ox��x=12�����Ըû����������������ʽ��ʾΪLi2OAl2O34SiO2�����Դ��ǣ�Li2OAl2O34SiO2����2���¶ȵ���250�棬��Ӧ���ʽ������¶ȸ���300�棬����ӷ��϶࣬��Ӧ�¶ȿ�����250��300�棬��Ӧ���ʽϿ죬��������ӷ���
�������������࣬���ĵ���࣬�����л���Ҫ��ȥ���������ᣬ���Ӻ������ʵĴ����������Ӻ����к���ĸ�����
���Դ��ǣ��¶ȵ���250�棬��Ӧ���ʽ������¶ȸ���300�棬����ӷ��϶ࣻ�����л���Ҫ��ȥ���������ᣬ���Ӻ������ʵĴ����������Ӻ����к���ĸ�������3��ˮ��ʱ������CaCO3��ĩ��ַ�Ӧ����ˣ���������Ҫ�ɷֳ�CaCO3���CaSO4��SiO2��Al��OH��3��
���Դ��ǣ�CaSO4��SiO2��Al��OH��3����4������ﮡ�������̼������Li2SO4��Ӧ����Li2CO3 �� ��Ӧ����ʽΪ��Na2CO3+Li2SO4=Li2CO3��+Na2SO4 ��
���Դ��ǣ�Na2CO3+Li2SO4=Li2CO3��+Na2SO4����5���¶�Խ�ߣ�̼����ܽ�Ƚ��ͣ�����̼����ܽ⣬�������Ӳ��ʣ���Һ�������Ʋ���Ӧ��ʹ�õ�̼����Ҫ����������̼����ܽ�����Һ�У�����̼�������ĸҺ����Ҫ���������ƣ������ܺ���̼���ơ�̼��ﮣ�
���Դ��ǣ��¶�Խ�ߣ�̼����ܽ�Ƚ��ͣ��������Ӳ��ʣ�̼���ƣ�̼��ﮣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���з�Ӧ���Ȼ�ѧ����ʽΪ��
1��C��s��+O2��g��=CO2��g����H1=��393.5kJ/mol
2��CH3COOH��l��+2O2��g��=2CO2��g��+2H2O��l����H2=��870.3kJ/mol
3��H2��g��+ ![]() O2��g��=H2O��l����H3=��285.8kJ/mol
O2��g��=H2O��l����H3=��285.8kJ/mol
��Ӧ2C��s��+2H2��g��+O2��g��=CH3COOH��l�� �ķ�Ӧ�ȣ��ʱ䣩Ϊ�� ��
A.+488.3kJ/mol
B.��488.3kJ/mol
C.��244.15kJ/mol
D.+244.15kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������зḻ��ʳƷ���������Դ��ҩ���ˮ������Դ����ͼ��ʾ��ˮ�ۺ����õIJ��ֹ��̣�����˵������ȷ���ǣ� �� 
A.��ҵ��ͨ���������״̬MgCl2��ȡ����þ
B.�ó���ʯ��ˮ�ɼ���NaHCO3��Na2CO3
C.�ڵڢڡ��ܲ����У���Ԫ�ؾ�������
D.��ȡNaHCO3�ķ�Ӧ�У����������ܽ������ͬ������С��NaCl������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ⱦ������Ҫ��SO2�йص���
A. ˮ��B. ������ն�
C. ����D. ��ɫ��Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.1mol/L��H2C2O4��Һ��H2C2O4��HC2O4����C2O42����������ռ���ʵ����������ֲ�ϵ������pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�������ȷ���ǣ� �� 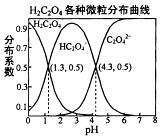
A.HC2O4��H++C2O42�� �� K=1��10��4.3
B.�������ʵ�����NaHC2O4��NAa2C2O4����ˮ�У�������ҺPHǡ��Ϊ4.3
C.������HF��KB=1��10����3.45 �� ������H2C2O4��Һ���뵽����NaF��Һ�У������ķ�ӦΪ��H2C2O4+F��=HF+HC2O4��
D.��0.1mol/LNaHC2O4��Һ�У�������Ũ�ȴ�С��ϵΪ��c��Na+����c��HC2O4������c��C2O42������c��OH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ������У�����������Ҫ��¼һЩʵ������ݣ��������ݿ��ŵ��ǣ�
A. ij����������ܶ�Ϊ2.8 g��cm��3
B. ��������ƽ�Ƴ����������Ϊ7.85 g
C. ij������ˮ��pHΪ5.6
D. Ba(OH)2��8H2O������NH4Cl�����Ͻ������¶�����5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ�û���ʵ�뽺�������û�й�ϵ����
A. ��������������ˮ
B. ��ʯ�����±���ƶ���
C. ��FeCl3��Һ�еμ�NaOH��Һ���ֺ��ɫ����
D. �峿�������ï�ܵ���ľ֦Ҷ���������������������Ĺ��ߣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ѧ��ʵʩ��һ������ɫ�ƻ�����ͨ����������̼�õ�̼���ϣ�����ԭ����ͼ��ʾ���������õõ���̼������������ӵ�أ�����˵����ȷ���ǣ� �� 
A.ͼ����������ʽֻ��һ��
B.�����ĵ缫��ӦʽΪ2CO32����4e��=2CO2��+O2��
C.����Ӧ��ת��1mole�� �� ������������CO32��0.5mol
D.������12g̼����ʱ�����ռ���22.4L O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�Ħ��������˵������ȷ����
A. CO2��Ħ����������������Է�������
B. H2��Ħ������������6.02��1023���������ӵ�����
C. H2O��Ħ������Ϊ18g
D. Al(OH)3��Na2O2��Ħ��������ͬ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com