
【题目】我国科学家研发了一种室温下“可呼吸”的Na-CO2二次电池。将NaClO4溶于有机溶剂作为电解液,纳和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() Na2CO3+C。下列说法错误的是( )
Na2CO3+C。下列说法错误的是( )
A.放电时,ClO4-向负极移动
B.放电时,Na+向正极移动
C.放电时,正极反应为:3CO2+3e-=2CO32-+C
D.放电时,正极反应为:Na++e-=Na
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】25℃时,向0.1mol/LNH3·H2O溶液中通入HCl气体,溶液中![]() 与pOH(仿pH定义)的关系如图所示。下列有关叙述正确的是
与pOH(仿pH定义)的关系如图所示。下列有关叙述正确的是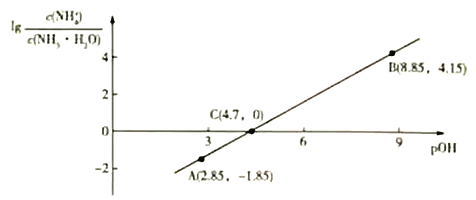
A. C点的溶液中:c(NH3·H2O)>c(NH4+)
B. pOH=7的客液中的溶质是NH4Cl
C. pOH=3的客液中:c(NH4+)+c(H+)+c(NH3·H2O)-c(OH-)=0.1mol/L
D. NH3·H2O的Kb=1.0×10-4.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列有关说法中正确的是
A.60 g乙酸分子中所含共价键的数目为 8NA
B.标准状况下,11.2LCHCl3中含有的原子总数为2.5NA
C.高温下,1mol Fe与足量水蒸气反应,转移电子数的目为3 NA
D.将1molCl2通入水中,所得溶液中HClO、Cl-、ClO-粒子数之和为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国在太阳能光电催化-化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是(已知质子交换膜只允许H+通过)( )
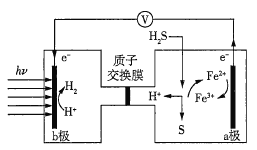
A.该制氢工艺中光能最终转化为化学能
B.该装置工作时,H+由b极区流向a极区
C.a极上发生的电极反应为Fe3++e-=Fe2+
D.a极区需不断补充含Fe3+和Fe2+的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.  Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.  正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
C.  锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
D.  使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华人民共和国国家标准(GB27602011)规定葡萄酒中SO2最大使用量为0.25g·L-1。某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。


(1)仪器A的名称是_________,水通入A的进口为________。(a/b)
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为__________________。
(3)除去C中过量的H2O2,然后用0.0900mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择题图2中的______ (填序号);若滴定终点时溶液的pH=8.8,则选择的指示剂为_________(酚酞/甲基橙);若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积____(填序号)(①=10mL,②=40mL,③<10mL,④>40mL)。
(4)滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为_______g·L-1。
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用钌(Ru)基催化剂催化CO2(g)和H2(g)的反应时,每生成92g液态HCOOH放出62.4kJ的热量,下列说法正确的是( )

A.图示中物质II为该反应的催化剂
B.图示中参与循环的物质只有CO2和H2
C.反应的活化能为62.4kJ·mol-1
D.该反应的热化学方程式为H2(g)+CO2(g)=HCOOH(l) △H=-31.2kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴、铜及其化合物用途非常广泛。回答下列问题:
(1)基态Br原子核外电子排布式为[Ar]___。
(2)已知反应:Cu(BF4)2.6H2O+Cu+8CH3CN=2[Cu(CH3CN)4]BF4+6H2O。
①配合物[Cu(CH3CN)4]BF4中,与铜形成配位键的原子是___,BF4-的空间构型是___,与BF4-互为等电子体的分子有___(任写一种)。
②CH3CN分子中碳原子的杂化方式是___;1个CH3CN分子中含有___个σ键。
(3)电子亲合能与电离能相对应,元素的气态基态原子获得一个电子成为气态一价负离子所释放的能量称为该元素的第一电子亲合能,其大小主要取决于原子的有效核电荷、原子半径和原子的电子构型等因素。Br与F、Cl位于同一主族,第一电子亲合能(如图1所示)原比氯和溴都小,其原因是___。
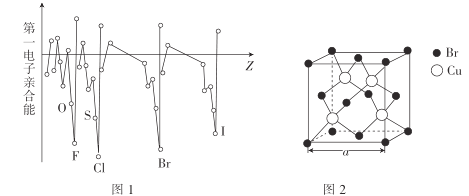
(4)溴化亚铜(晶胞结构如图2所示)可用作有机合成的催化剂,密度为4.71g·cm-3。
①晶胞中Br-的配位数为___。
②晶胞参数a=___(列出表达式即可)nm。(设NA为阿伏加德罗常数的数值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物K是某药物的合成中间体,其合成路线如图所示: 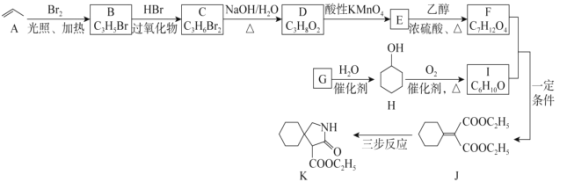
已知:①R1-NH2+R2-COOC2H5![]()
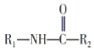 +C2H5OH(R表示烃基或氢原子);
+C2H5OH(R表示烃基或氢原子);
②R-CN ![]() R-CH2NH2(R表示烃基);
R-CH2NH2(R表示烃基);
③HBr与不对称烯烃加成时,在过氧化物作用下,则卤原子连接到含氢较多的双键碳上。
请回答下列问题:
(1)C的化学名称为_____。
(2)D→E的反应类型为_____,F中官能团的名称是_____。
(3)G→H的化学方程式为_____。
(4)J的分子式为________。手性碳原子是指与四个各不相同原子或基团相连的碳原子,则K分子中的手性碳原子数目为_____。
(5) L是F的同分异构体,则满足下列条件的L的结构简式为_________。(任写一种结构即可)
A. 1 mol L与足量的NaHCO3溶液反应能生成2 mol CO2;
B. L的核磁共振氢谱有3组峰且峰面积之比为1:2:3。
(6)请写岀J经三步反应合成K的合成路线:_____(无机试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com