
将煤直接作为燃料燃烧,不但热效率较低,且产生烟尘、二氧化硫、氮的氧化物等,带来严重的环境污染。煤干馏是提高煤利用率、生产重要化工原料、降低污染物排放量的有效措施之一。
某化学学习小组在实验室条件下探究煤干馏的现象及产物,装置如图,请回答有关问题:
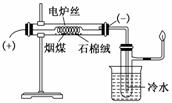
(1)煤干馏的条件是________________________________________________________;
(2)盛有冷水的烧杯的作用是_______________________________________________;
(3)实验后检验生成粗氨水的操作是_______________________________________
________________________________________________________________________;
(4)已知CO不能使溴水褪色,若将从具支试管出来的气体通入溴水中,发现溴水褪色,则说明产生了________;
(5)检验从具支试管出来的气体的性质后,将尾气点燃,火焰的颜色为________;
(6)从煤焦油中分离出苯及其同系物的实验方法是___________________
________________________________________________________________________。
科目:高中化学 来源: 题型:
下列实验装置设计正确、且能达到目的的是 
A.实验Ⅰ:制备金属钠 B.实验Ⅱ:制取氢氧化亚铁并观察其颜色
C.实验Ⅲ:制取少量的氢氧化铝 D.实验Ⅳ:比较两种物质的热稳定 性
性
查看答案和解析>>
科目:高中化学 来源: 题型:
以下反应最符合绿色化学原子经济性要求的是( )
A.乙烯聚合为聚乙烯高分子材料
B.甲烷与氯气制备一氯甲烷
C.以铜和浓硝酸为原料生产硝酸铜
D.用SiO2制备高纯硅
查看答案和解析>>
科目:高中化学 来源: 题型:
“绿色化学”是人们最近提出的一个新概念,主要内容之一是指从技术上、经济上设计可行的化学反应,尽可能减少对环境的负作用。下列化学反应不符合绿色化学概念的是( )
A.消除硫酸厂尾气中的SO2:SO2+2NH3+H2O===(NH4)2SO3
B.消除硝酸工业尾气的氮氧化物的污染:NO+NO2+2NaOH===2NaNO2+H2O
C.制CuSO4:Cu+2H2SO4(浓)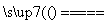 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D.制 CuSO4:2Cu+O2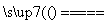 2CuO;CuO+H2SO4===CuSO4+H2O
2CuO;CuO+H2SO4===CuSO4+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4; ②1s22s22p63s23p3; ③1s22s22p3; ④1s22s22p5。则下列有关比较中正确的是
A.第一电离能:①>② B.原子半径:④>③
C.电负性: ②>③ D.氢化物稳定性:①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 需要加热方能发生的反应一定是吸热反应 B.放热反应在常温下一定很容易发生
C.反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小
D.化学反应只生成新物质,没有能量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇可通过将煤气化过程中生成的CO和H2在一定条件下,发生如下反应制得:CO(g)+2H2(g)  CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题:

(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=________,CO的转化率为________。
(2)该反应的平衡常数表达式为________________,温度升高,平衡常数________(填“增大”、“减小”或“不变”)。
(3)若在一体积可变的密闭容器中充入1 mol CO、2 mol H2和1 mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则加入各物质后该反应向________(填“正”或“逆”)反应方向移动,理由是___________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com