
����Ŀ������AG��ʾ��Һ����ȣ������ʽΪ��AG=lg[ ]�������£�ʵ��������0.10 mol/L ��������Һ�ζ�10 mL 0.10 mol/L MOH��Һ���ζ�������ͼ��ʾ������˵����ȷ����
]�������£�ʵ��������0.10 mol/L ��������Һ�ζ�10 mL 0.10 mol/L MOH��Һ���ζ�������ͼ��ʾ������˵����ȷ����

A. �õζ����̿�ѡ���̪��Ϊָʾ��
B. C�������������Ϊ10mL
C. ��B������������Һ���Ϊ5mL��������Һ�У�c(M+)+2c(H+)=c(MOH)+2c(OH)
D. �ζ������д�A�㵽D����Һ��ˮ�ĵ���̶�������
���𰸡�C
�������������������ͼ���֪��0.10 mol/L MOH��Һ�����Ϊ-8����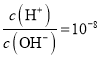 ������ˮ�����ӻ����������������Һ��c(OH-)=10-3mol/L������MOHΪ���A. �����ǡ�÷�Ӧʱ��������ҺΪǿ����������Һ������Һ�����ɵ���ˮ��������ԣ�����Ӧѡ����ȽϺ��ʣ�������ʵ������С��A����ȷ��B. C���Ӧ����Һ��pH=7����Һ�����ԣ����Լ�����������С��10mL��B����ȷ��C. ��B������������Һ���Ϊ5mL����������������ʵ�����MOH��һ�룬�������غ��c(M+)+ c(MOH) = 2c(Cl)���ɵ���غ��c(M+)+c(H+)= c(Cl)+c(OH)����ˣ�������Һ��c(M+)+2c(H+)=c(MOH)+2c(OH)��C��ȷ��D. �ζ������д�A�㵽D����Һ��ˮ�ĵ���̶�����������������С��D����ȷ������ѡC��
������ˮ�����ӻ����������������Һ��c(OH-)=10-3mol/L������MOHΪ���A. �����ǡ�÷�Ӧʱ��������ҺΪǿ����������Һ������Һ�����ɵ���ˮ��������ԣ�����Ӧѡ����ȽϺ��ʣ�������ʵ������С��A����ȷ��B. C���Ӧ����Һ��pH=7����Һ�����ԣ����Լ�����������С��10mL��B����ȷ��C. ��B������������Һ���Ϊ5mL����������������ʵ�����MOH��һ�룬�������غ��c(M+)+ c(MOH) = 2c(Cl)���ɵ���غ��c(M+)+c(H+)= c(Cl)+c(OH)����ˣ�������Һ��c(M+)+2c(H+)=c(MOH)+2c(OH)��C��ȷ��D. �ζ������д�A�㵽D����Һ��ˮ�ĵ���̶�����������������С��D����ȷ������ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ķ�չ�����У�����������Ҫ�����ã�����˵����ȷ���ǣ� ��
A.�����Ͼ����������Ԫ����������̬��������Ȼ���е�
B.�ڻ�ѧ��Ӧ�У���������ʧȥ���ӣ��ǻ�ԭ��
C.�����Ͻ���۵����������ijɷֵĽ������۵�
D.�赥�������õİ뵼�壬�������ǽ���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������У���ȷ���ǣ� ��
A.CCl4���ӵ����ģ�ͣ� ![]()
B.![]() ����̼ԭ�ӿ�����ͬһƽ����
����̼ԭ�ӿ�����ͬһƽ����
C.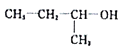 ����Ϊ2-��-1-����
����Ϊ2-��-1-����
D.��ȩ������ϩ���Ҷ���������Ϊ�ϳɾۺ���ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ƻ����Ľṹ��ʽΪ�� ![]() ������˵����ȷ���ǣ� ��
������˵����ȷ���ǣ� ��
A.ƻ�����ܱ���������Ԫ����
B.1 molƻ�������3 mol NaOH�����кͷ�Ӧ
C.��1 molƻ�����ϡ��Һ����������Na��Ӧ����1.5molH2
D.2����ƻ�������Ӧ�����γɽṹΪ��Ԫ������Ԫ�����Ԫ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A. Ԫ�صĵ�һ������Խ���������һ��Խǿ
B. Ԫ�صĵ�һ������ԽС���������һ��Խǿ
C. �������ʸ��ᷴӦ�����ף�ֻ���ý���Ԫ�صĵ�һ�������й�
D. �������ʸ��ᷴӦԽ���ף�����Ԫ�صĵ縺��ԽС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���У�1H,2H,3H������ͬλ�أ����У�35Cl,37Cl������ͬλ�أ��á���ȷ����ƽ���ֱ����1000��HCl���ӣ��������ݿ����У� ��
A.1��
B.5��
C.6��
D.1000��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬһ�������Ҳ����Ҫ�İ뵼����ϣ���Ӧ���ں��պ����ء�����ͨѶ������һ���ᴿ���������Ʒ����Ҫ��GeO2��As2O3���Ĺ������£�

��֪���١�����������еķ�ӦΪ��GeO2��2NaOH��Na2GeO3��H2O��As2O3��2NaOH��2NaAsO2��H2O
�� GeCl4���۵�Ϊ-49.5�棬AsCl3��GeCl4�ķе�ֱ�Ϊ130.2�桢84�档
��1�����ԭ������Ϊ33������Ԫ�����ڱ��е�λ��Ϊ��______���ڵ�________�塣
��2�����������顱�Ĺ����ǽ�NaAsO2����ΪNa3AsO4���䷴Ӧ�����ӷ���ʽΪ��___________________________________________________________________��
��3����ͳ���ᴿ�����ǽ���Ʒֱ�Ӽ���������������ȱ����_________________��
��4�����������еķ�Ӧ�Ļ�ѧ����ʽΪ��________________________________��
��5����ˮ�⡱����ʱ���ֽϵ��¶���������߲��ʣ�������ܵ�ԭ����_____________����һ�����ɣ���
��6����1�ֶ��������Ʒ��������30%�����ᴿ��0.745�ֵĽϴ����������Ʒ���������ѳ���Ϊ_________��
��7������ͬһ�������Ҳ�������ڰ뵼���С�һ��ͻ�ƴ�ͳ�����������þ����Һ̬�������ε�ع���ԭ����ͼ��ʾ��

�õ�������ܶȵIJ�ͬ�������������·�Ϊ���㣬����ʱ�м�������ε���ɲ��䡣���ʱ��C1����______����ϡ����¡����ƶ����ŵ�ʱ�������ĵ缫��ӦʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1 mol ���ۼ������յ��������γ�1 mol ���ۼ����ͷŵ�������Ϊ���ܡ���֪��H��H����Ϊ436 kJ /mol��H��N����Ϊ391 kJ /mol�� N2 (g)+ 3H2(g) ![]() 2NH3(g) ��H����92.4 kJ /mol������˵������ȷ����(����)
2NH3(g) ��H����92.4 kJ /mol������˵������ȷ����(����)
A. H��H��N��N���ι�
B. N��N����ԼΪ946 kJ/mol
C. �ϳɰ���Ӧѡ���ʵ��Ĵ�����Ϊ�����H2��ת����
D. 0.5 mol N2��1.5 mol H2����������³�ַ�Ӧ���ų�����Ϊ46.2 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪:��![]() ��
��![]() ��
��![]() �ķ���ʽ��ΪC8H8������˵����ȷ����
�ķ���ʽ��ΪC8H8������˵����ȷ����
A. �٢ڢ۵����ȴ��������ȴ����ͬ���칹����Ŀ��ͬ
B. �٢ڢ۾���ʹ���Ը��������Һ������ѧ��Ӧ����ɫ
C. �ڷ���������ԭ��һ����ͬһƽ����
D. ����̼���ļۿ��ǣ��ٵ�ͬ���칹��ֻ�Тں͢�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com