
分析 (1)①根据溶液的配制过程选择仪器;
②NaOH溶液应该用碱式滴定管量取;
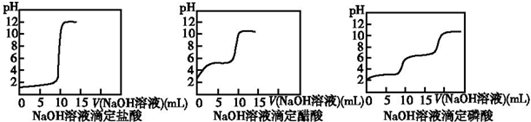
(2)根据图象可知酸性越强,其pH变化越快;
②醋酸恰好中和时得到醋酸钠溶液,醋酸根离子水解显示碱性,根据盐类的水解原理分析;
③NaOH滴定磷酸时,消耗NaOH的量多.
解答 解:(1)①根据溶液的配制过程选择仪器,在定容时需要胶头滴管,用到的仪器是:250mL容量瓶、胶头滴管、量筒;故答案为:250mL容量瓶、胶头滴管、量筒;
②NaOH溶液能腐蚀酸式滴定管中的活塞,所以要用碱式滴定管,故答案为:碱式;
(2)①根据图象可知酸性越强,其pH变化越快,所以其酸性由强到若的顺序为:盐酸>磷酸>醋酸,故答案为:盐酸>磷酸>醋酸;
②醋酸与氢氧化钠反应生成CH3COONa为强碱弱酸盐,水解显碱性,所以其水溶液PH大于7,即CH3COO-+H2O?CH3COOH+OH-,故答案为:CH3COO-+H2O?CH3COOH+OH-;
③NaOH滴定磷酸时,消耗NaOH的量多,氢氧化钠的用量超过了碱式滴定管的最大体积读数,故答案为:不可行;中和后生成的醋酸钠水解使溶液显碱性.
点评 本题考查了中和滴定实验,以及弱酸的电离,盐类的水解,难度中等,要注意滴定管的选择.


科目:高中化学 来源: 题型:解答题
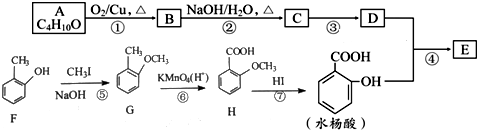
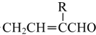
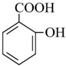 →
→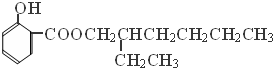 +H2O;
+H2O;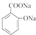
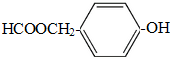 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
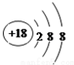
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2、NO2均为酸性氧化物 | B. | 石英、水玻璃均为纯净物 | ||
| C. | NaCl、BaSO4均为强电解质 | D. | 烧碱、纯碱均为碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HA较强 | B. | HB较强 | C. | 两者一样 | D. | 无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42-+2 Ba2++4OH-=AlO2-+2BaSO4↓+2H2O | |
| B. | 向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+=Fe2++2H2O | |
| C. | 向磷酸二氢铵溶液中加入足量的氢氧化钠溶液:NH4++OH-=NH3•H2O | |
| D. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-$\stackrel{△}{→}$CH2BrCOO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
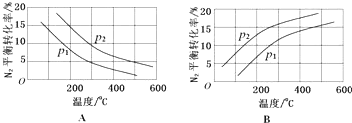
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| X | Y | ||
| W | Q |
| A. | 简单离子半径大小关系为:W>Z>Y | |
| B. | 核外最外层电子数:Q>Y>X>W>Z | |
| C. | X与氢元素形成的化合物中,只含极性键 | |
| D. | 常见单质的熔沸点:X>W>Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com