
【题目】CO2 的的资源化利用是解决温室效应的重要途径。以下是在一定条件下用 NH3捕获 CO2生成重要化工产品三聚氰酸的反应:NH3+CO2→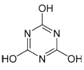 +H2O。下列有关三聚氰酸的说法正确的是( )
+H2O。下列有关三聚氰酸的说法正确的是( )
A.C、N、O 原子采用相同的杂化方式B.分子中既含极性键,又含非极性键
C.分子式为C3H3N3O3D.生成该物质的上述反应为中和反应
科目:高中化学 来源: 题型:
【题目】工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(1)用双线桥表示出电子转移的方向和数目__,题干中反应改写成离子方程式是___。
(2)电解食盐水的过程中,氧化产物是___。
(3)电解食盐水要求对粗食盐水进行精制,以除去租食盐水中含有的泥沙和SO42-、Ca2+,Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。盐酸与滤液反应的离子方程式:___,___。
(4)请配平以下化学方程式:__Al+__NaNO3+__NaOH=__NaAlO2+__N2↑+__H2O。若反应过程中转移5mol电子,则生成标准状况下N2的体积为___L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有amol AlCl3溶液中加入含有bmol KOH溶液,生成沉淀的物质的量可能是
①amol ②bmol ③a/3mol ④b/3mol ⑤0 mol ⑥(4a-b)mol
A.①③④⑤⑥B.①②③④⑤C.①④⑤⑥D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是应用最广泛的金属,铁的氯化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)在实验室中,FeCl2可用铁粉和___(填名称)反应制备。
(2)Fe3O4可用多种方法制得,其中由一种单质和一种化合物通过化合反应制备的化学方程式为___。
(3)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是___,对应的化学方程式为___。
(4)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe3+:___。
(5)现有一含有FeCl2和FeCl3的混合物样品,实验测得n(Fe):n(C1)=1:2.1,则该样品中FeCl3的物质的量分数为___。
(6)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图(如图),回答下列问题。

(1)操作Ⅰ中所用的仪器有____。
(2)固体A的成分是___和____。(填名称);操作Ⅲ是____。
(3)如何检验溶液a中主要阴离子____。
(4)回收的铜可以用于制备胆矾(CuSO4·5H2O)。将铜和0.22mol/LH2SO4溶液混合后,在加热的情况下不断通入氧气就可以制得CuSO4,然后将所得的溶液经过“一系列操作”后得到胆矾。写出生成CuSO4的化学方程式:___。
(5)某同学用密度为1.84g/cm3、质量分数为 98%的浓硫配制500mL0.22mol/L的稀硫酸溶液,需要用规格为___mL的量筒量取___mL的浓硫酸。
(6)配制该溶液的过程中,下列操作使得所配得的溶液浓度偏小的是___(填字母)。
A.稀释密度为1.84g/cm3、质量分数为 98%的浓硫酸时,不小心溅出少量硫酸溶液
B.用蒸馏水洗涤烧杯、量筒及玻璃棒,并将洗涤液注入容量瓶中
C.定容时反复上下倒转容量瓶后,发现凹液面最低处低于刻度线,再补加水到刻度线
D.量取密度为1.84g/cm3、质量分数为 98%的浓硫酸时,仰视量筒的刻度线
E.洗涤容量瓶后,立即用来配制溶液
F.稀释浓硫酸结束后立即将溶液转移到容量瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3CuO+2NH3![]() 3Cu+N2+3H2O。下列判断正确的是
3Cu+N2+3H2O。下列判断正确的是
A.N元素的化合价降低B.NH3被还原
C.消耗0.3 mol CuO转移0.6 NA个电子D.CuO是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
(1)溶于海水的CO2主要以4种无机碳形式存在,其中HCO3-占95%,写出CO2溶于水产生HCO3-的方程式:_____________。
(2)在海洋循环中,通过如图所示的途径固碳。
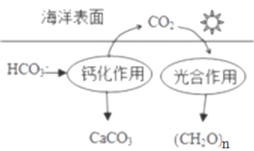
①写出钙化作用的离子方程式:_____________。
②同位素示踪法证实光合作用释放出的O2只来自于H2O,用18O标记物质的光合作用的化学方程式如下,将其补充完整:_____________+_____________=(CH2O)x+x18O2+xH2O,_____________
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
①气提、吸收CO2,用N2从酸化后的海水中吹出CO2并用碱液吸收(装置示意图如图所示),将虚线框中的装置补充完整并标出所用试剂。_____________

②滴定。将吸收液洗后的无机碳转化为NaHCO3,再用xmol/LHCl溶液滴定,消耗ymLHCl溶液,海水中溶解无机碳的浓度=_____________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_____________________。
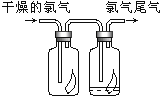
(2)为防止氯气尾气污染空气,实验室通常用______溶液吸收多余的氯气,原理是__________________。
(用化学方程式表示)。
根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是______(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是______(填字母,下同)。
A.O2 B.Cl2 C.CO2 D.HClO
(3)一旦发生氯气泄漏和爆炸事故,周围群众应紧急疏散。当人们逃离爆炸现场时,可以用浸有一定浓度某物质水溶液的毛巾捂住鼻子,最适宜采用的该物质是_____________。
A.NaOH B.NaCl C.KCl D.Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com