
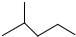
 表示的分子式结构简式名称是C6H14、(CH3)2CHCH2CH2CH3、2-甲基戊烷.
表示的分子式结构简式名称是C6H14、(CH3)2CHCH2CH2CH3、2-甲基戊烷.| 实验步骤 | 解释或实验结论 |
| (1)称取A物质 18.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空: ?A的相对分子质量为:90 |
(2)A的核磁共振氢谱如图: | ?A中含有4种氢原子 |
分析 (1) 分子中含有6个碳原子,属于饱和烃,分子式为C6H14,依据烷烃的命名原则命名,依据键线式书写结构简式即可;
分子中含有6个碳原子,属于饱和烃,分子式为C6H14,依据烷烃的命名原则命名,依据键线式书写结构简式即可;
(2)蒸馏时需要的主要仪器有酒精灯、蒸馏烧瓶、冷凝管等;
(3)物质的相对分子质量之比等于相对密度,核磁共振氢谱有几个峰,则有几种H原子.
解答 解:(1) 分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,结构简式为:(CH3)2CHCH2CH2CH3,命名为:2-甲基戊烷,
分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,结构简式为:(CH3)2CHCH2CH2CH3,命名为:2-甲基戊烷,
故答案为:C6H14、(CH3)2CHCH2CH2CH3、2-甲基戊烷;
(2)含有杂质的工业乙醇的蒸馏装置中,需要使用的玻璃仪器为:酒精灯、蒸馏瓶、温度计、冷凝管、尾接管、锥形瓶,还缺少温度计和冷凝管,
故答案为:冷凝管;
(3)称取A物质 18.0g,升温使其汽化,测其密度是相同条件下H2的45倍,则相对分子质量为45×2=90,
A的核磁共振氢谱有4个峰,则有4种H原子,
故答案为:90;4.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握有机物的键线式与结构简式,把握有机物的分离、提纯方法,难度不大.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
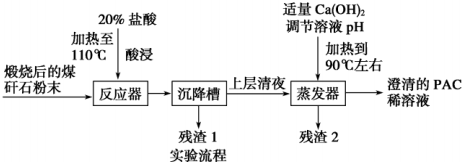
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
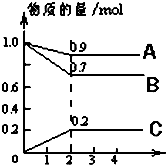 某温度时,在2L密闭容器中,A、B、C三种物质的物质的量随时间的变化曲线如图所示.由图中数据分析:
某温度时,在2L密闭容器中,A、B、C三种物质的物质的量随时间的变化曲线如图所示.由图中数据分析:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
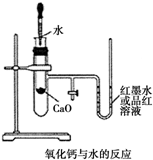 如图是某同学设计的放热反应的观察装置,其实验操作步骤如下:
如图是某同学设计的放热反应的观察装置,其实验操作步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
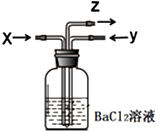 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )| A. | 洗气瓶中产生的沉淀是BaCO3 | B. | Z导管出来的气体中无CO2 | ||
| C. | 洗气瓶中产生的沉淀只有BaSO4 | D. | 洗气瓶中产生的沉淀可能有BaSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com