

| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 取步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
(12分)进行中和热的测定的装置如图所示。回答下列问题:
(1)从实验装置中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)利用该装置测得的中和热数值 (填“偏大、偏小、无影响”)
(4)某研究小组将装置完善后,把V1 mL 1.0 mol/LHCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示
(实验中始终保持V1+V2=50 mL)。回答下列问题:
①研究小组做该实验时环境温度 (填“高于”、“低于”或“等于”)22 ℃。
②由题干及图形可知,V1/V2= : 时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2013年全国普通高等学校招生统一考试理科综合能力测试化学(重庆卷带解析) 题型:实验题
某研究小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)
(1)MgCO3的分解产物为 。
(2)装置C的作用是 ,处理尾气的方法为 。
(3)将研究小组分为两组,按图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
查看答案和解析>>
科目:高中化学 来源:2013年全国普通高等学校招生统一考试理科综合能力测试化学(重庆卷解析版) 题型:实验题
某研究小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)

(1)MgCO3的分解产物为 。
(2)装置C的作用是 ,处理尾气的方法为 。
(3)将研究小组分为两组,按图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
|
步骤 |
操作 |
甲组现象 |
乙组现象 |
|
1 |
取黑色粉末加入稀盐酸 |
溶解,无气泡 |
溶解,有气泡 |
|
2 |
取步骤1中溶液,滴加K3[Fe(CN)6]溶液 |
蓝色沉淀 |
蓝色沉淀 |
|
3 |
取步骤1中溶液,滴加KSCN溶液 |
变红 |
无现象 |
|
4 |
向步骤3溶液中滴加新制氯水 |
红色褪去 |
先变红,后褪色 |
①乙组得到的黑色粉末是 ;
②甲组步骤1中反应的离子方程式为 ;
③乙组步骤4中,溶液变红的原因为 ;溶液褪色可能的原因及其验证方法为 ;
④从实验安全考虑,题9图装置还可采取的改进措施是 。
查看答案和解析>>
科目:高中化学 来源:2013届辽宁省高二上学期期中考试化学试卷 题型:实验题
(12分)进行中和热的测定的装置如图所示。回答下列问题:

(1)从实验装置中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)利用该装置测得的中和热数值 (填“偏大、偏小、无影响”)
(4)某研究小组将装置完善后,把V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示
(实验中始终保持V1+V2=50 mL)。回答下列问题:
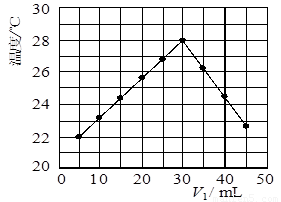
①研究小组做该实验时环境温度 (填“高于”、“低于”或“等于”)22 ℃。
②由题干及图形可知,V1/V2= : 时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为 mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com