
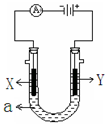


科目:高中化学 来源:不详 题型:单选题
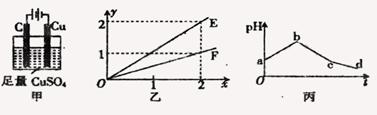
| A.OE表示反应生成CU的物质的量 |
| B.OF表示反应生成O2的物质的量 |
| C.bc 段阳极产物是Cl2 |
| D.cd段电解的物质是水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解精炼金属时,含杂质的粗金属做阳极,与电源正极相连 |
| B.电解池中金属导线中电子由电源的负极流向电解池的阳极,从电解池的阴极流向电源的正极 |
| C.在电解池中,电解质溶液中的阴离子向阴极移动,阳离子向阳极移动 |
| D.在电解精炼金属过程中,电解质溶液的成分不发生任何变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解熔融的氧化铝制取金属铝,用铁作阳极 | B.电解法精炼粗铜,用纯铜作阳极 |
| C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | D.在镀件上电镀锌,用锌作阴极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
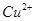 和
和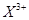 均为0.1mol的溶液,阴极析出金属的质量m(g)与电路中通过电子的物质的量
均为0.1mol的溶液,阴极析出金属的质量m(g)与电路中通过电子的物质的量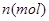 关系如图,则离子的氧化能力由大到小排列正确的是( )
关系如图,则离子的氧化能力由大到小排列正确的是( )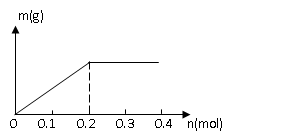
A.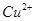 > >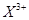 > >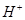 |
B.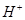 > >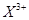 > >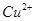 |
C.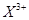 > >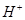 > >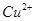 |
D.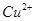 > >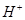 > >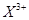 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com