
科目:高中化学 来源:不详 题型:填空题
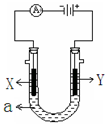
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
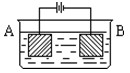
| A.3︰1 | B.4︰1 | C.2︰1 | D.任意比 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解熔融NaOH可生成金属钠、O2以及H2 |
| B.电解熔融CaCl2时,金属钙在阳极生成 |
| C.可用电解饱和MgCl2溶液的方法获得金属镁 |
| D.电解熔融Al2O3制备金属铝时,要加入冰晶石,使Al2O3在较低温度下熔解。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
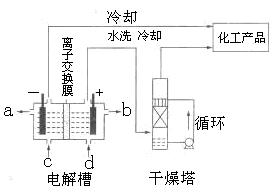
 4SiHCl3(g)
4SiHCl3(g) (标准状况)。
(标准状况)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
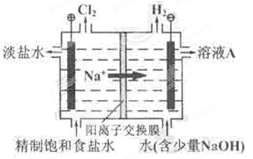
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com