
【题目】①1mol丙酮酸(  )在镍的催化下与1mol氢气发生加成反应转变成乳酸,则乳酸的结构简式为。
)在镍的催化下与1mol氢气发生加成反应转变成乳酸,则乳酸的结构简式为。
②在酸性条件下,与乳酸具有相同官能团的乳酸的同分异构体A发生消去反应生成B,则由A生成B的化学方程式为。
③B与甲醇生成的酯可以聚合,则该聚合物的结构简式为。
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案科目:高中化学 来源: 题型:
【题目】目前“低碳减排”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题.
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)2CO2(g)+N2(g).在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂表面积(S)和时间(I)的变化曲线如图所示.据此判断:
①该反应的△H0(填“>”或“<”).
②在T2温度下,0﹣2s内的平均反应速率v(N2)=mol/(Ls).
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是(填代号).
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
例如:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=﹣867kJmol﹣1
2NO2(g)═N2O4(g)△H=﹣56.9kJmol﹣1
写出CH4(g)催化还原N2O4(g)的热化学方程式: .
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.如图是通过人工光合作用,以CO2(g)和H2O(g)为原料制备HCOOH和O2的原理示意图.催化剂b表面发生的电极反应为 . 
③常温下0.1molL﹣1的HCOONa溶液pH为10,则HCOOH的电离常数Ka=molL﹣1(填写最终计算结果).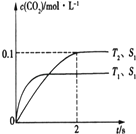
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 氯气有毒,实验室中用澄清石灰水吸收,防止污染空气
B. 天然气属于可再生能源
C. 碱石灰可以干燥氯气
D. 14C可用于文物年代的鉴定,14C与12C互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成.某校课外兴趣小组以两条途径分别对X进行如下实验探究.下列有关说法不正确的是( ) 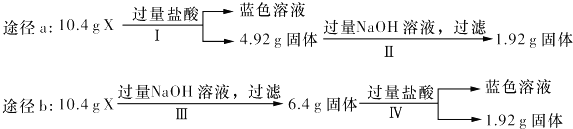
A.由工可知X中一定存在Fe2O3、Cu
B.无法判断混合物中是否含有Al2O3
C.1.92 g固体成分为Cu
D.原混合物中m( Fe2O3):m(Cu)=1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物(如NO2、NO4、N2O5等)应用很广,在一定条件下可以相互转化.
(1)从N2O5可通过电解或臭氧氧化N2O4的方法制备.电解装置如图1所示(隔膜用于阻止水分子通过),其阳极反应式为 .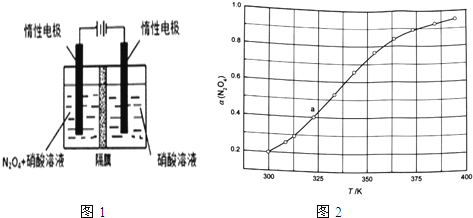
己知:2NO(g)+O2(g)═2NO2(g)△H1
NO(g)+O3(g)═NO2(g)+O2(g)△H2
2NO2(g)N2O4(g)△H3
2N2O5(g)═4NO2(g)+O2(g)△H4
则反应N2O4(g)+O3(g)═N2O5(g)+O2(g)的△H= .
(2)从N2O5在一定条件下发生分解:2N2O5(g)═4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
c(N2O5)/mol/L | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
设反应开始时体系压强为P0 , 第2.00min时体系压强为p,则p:p0= ;
1.00~3.00min内,O2的平均反应速率为 .
(3)从N2O4与NO2之间存在反应N2O42NO2(g).将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图1所示.
①图中a点对应温度下,已知N2O4的起始压强p0为108kPa,列式计算该温度下反应的平衡常数Kp= (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
②由图推测N2O4(g)2NO2(g)是吸热反应还是放热反应,说明理由 ,若要提高N2O4转化率,除改变反应温度外,其他措施有 (要求写出两条).
③对于反应N2O4(g)2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1p(N2O4),v(NO2)=k2[p(NO2)]2 . 其中,kl、k2是与反应及温度有关的常数.相应的速率一压强关系如图所示:一定温度下,kl、k2与平衡常数Kp的关系是kl= ,在图标出的点中,指出能表示反应达到平衡状态的点并说明理由 .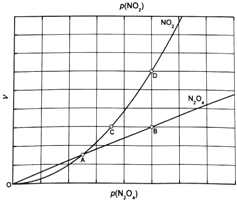
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《汉书》记载“高奴县有洧水,肥可燃”;《梦溪笔谈》描述“洧水”:“予疑其烟可用,试扫其煤以为墨,黑光如漆,松墨不及也……此物后必大行于世.”上述“洧水”和“煤”的主要成分分别是( )
A.石油和炭黑B.石油和焦炭
C.油脂和木炭D.油脂和石墨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠离子电池具有资源广泛、价格低廉、环境友好、安全可靠的特点,特别适合于固定式大规模储能应用的需求.一种以Na2SO4水溶液为电解液的钠离子电池总反应为:NaTi2(PO4)3+2 Na2NiFeII (CN)6![]() Na3Ti2(PO4)3+2NaNiFeIII(CN)6(注:其中P的化合价为+5,Fe的上标Ⅱ、Ⅲ代表其价态).下列说法不正确的是( )
Na3Ti2(PO4)3+2NaNiFeIII(CN)6(注:其中P的化合价为+5,Fe的上标Ⅱ、Ⅲ代表其价态).下列说法不正确的是( )
A.放电时NaTi2(PO4)3在正极发生还原反应
B.放电时负极材料中的Na+脱离电极进入溶液,同时溶液中的Na+嵌入到正极材料中
C.充电过程中阳极反应式为:2NaNiFeIII(CN)6+2Na++2e﹣=2Na2NiFeII (CN)6
D.该电池在较长时间的使用过程中电解质溶液中Na+的浓度基本保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学是日渐为人们所熟悉的社会概念。关于绿色食品的基本标准有如下几种说法,其中符合绿色食品要求的是( )
①香甜可口 ②无污染 ③表面呈绿色 ④无化学添加剂 ⑤有营养价值
A.①②③⑤
B.①③④⑤
C.②④⑤
D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的分子式为C51H96O6 , 在硫酸存在下发生水解A+3H2O ![]() B+2D+E,其生成物B与等物质的量的氢气完全加成可得到D;又知有机物E的相对分子质量为92,1molE与足量的钠反应可生成H233.6L(标准状况)。试回答:
B+2D+E,其生成物B与等物质的量的氢气完全加成可得到D;又知有机物E的相对分子质量为92,1molE与足量的钠反应可生成H233.6L(标准状况)。试回答:
(1)B的结构简式是 , E的名称是。
(2)A可能的结构有种,写出其中一种同分异构体的结构简式:。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com