
【题目】(1)比较熔点:![]() 晶体_______白磷晶体(填“>”、“<”或“=”),判断的理由是_______________;
晶体_______白磷晶体(填“>”、“<”或“=”),判断的理由是_______________;
(2)酸碱质子理论认为,能电离出质子(氢离子)的物质是酸,能结合质子的物质是碱,用一个离子方程式说明:![]() 与
与![]() 的碱性强弱________________;
的碱性强弱________________;
(3)一水合氨![]() 分子中,
分子中,![]() 与
与![]() 实际上是通过氢键相结合,请结合一水合氨的性质,用结构式画出一水合氨最有可能的分子结构____________。
实际上是通过氢键相结合,请结合一水合氨的性质,用结构式画出一水合氨最有可能的分子结构____________。
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的NO(g)和足量C(s),发生反应C(s)+2NO(g) ![]() CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )

A. 该反应的ΔH>0
B. 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
C. 在T2时,若反应体系处于状态D,则此时一定有v正<v逆
D. 在T3时,若混合气体的密度不再变化,则可以判断反应达到平衡状态C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上由含铜废料(含有Cu、CuS、CuSO4等)制备硝酸铜晶体的流程如图:
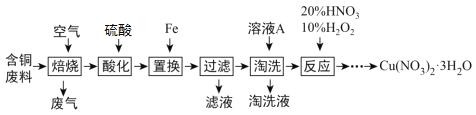
(1)“焙烧”时CuS转化为CuO和SO2,反应的化学方程式为___。
(2)“酸化”步骤反应的离子方程式为___。
(3)“过滤”所得滤液中溶质的主要成分为___。
(4)“淘洗”所用的溶液A应选用___(填序号)。
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”一步的过程中无红棕色气体生成。
①理论上消耗HNO3和H2O2的物质的量之比为___。
②若不加10% H2O2,只用浓HNO3,随着反应的进行,容器内持续出现大量红棕色气体,写出该反应的离子方程式____。
(6)由“反应”所得溶液中尽可能多地析出Cu(NO3)2·3H2O晶体的方法是___。(相关物质的溶解度曲线如图所示)
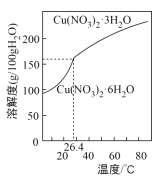
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() ,25℃时,
,25℃时,![]() 的
的![]() 。该温度下用
。该温度下用![]() 溶液滴定
溶液滴定![]() 溶液的滴定曲线如图所示。下列说法不正确的是( )
溶液的滴定曲线如图所示。下列说法不正确的是( )
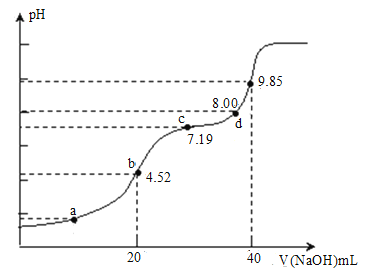
A.若a点溶液c(![]() )=c(H2SO3),则a点对应的
)=c(H2SO3),则a点对应的![]()
B.若选择b为反应终点,宜选择甲基橙为指示剂
C.c点对应的溶液2c(Na+)=3c(![]() )
)
D.d点对应的溶液c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种重要的清洁能源。
(1)航天员呼吸产生的![]() 利用
利用![]() 反应:
反应:![]() H,再电解水可实现
H,再电解水可实现![]() 的循环利用。
的循环利用。
①热力学中规定,由最稳定单质生成![]() 某物质的焓变称为该物质的标准生成焓(符号:
某物质的焓变称为该物质的标准生成焓(符号:![]() ),最稳定单质的标准生成焓规定为0。已知上述反应式中:
),最稳定单质的标准生成焓规定为0。已知上述反应式中:
![]() ;
;![]() ;
;![]() ;
;
![]() ;则
;则![]() _____
_____![]() 。
。
②![]() 反应必须在高温下才能进行,原因是___________________________。
反应必须在高温下才能进行,原因是___________________________。
③350℃时,向体积为![]() 的恒容密闭容器中通入
的恒容密闭容器中通入![]() 和
和![]() 发生以上反应。
发生以上反应。
测得反应过程中压强随时间的变化如下表所示:
时间/ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
压强 |
|
|
|
|
|
|
|
350℃时![]() 反应的
反应的![]() ______(
______(![]() 为用气体的分压代替各组分平衡浓度表示的平衡常数,气体分压=气体的体积分数×体系总压)。
为用气体的分压代替各组分平衡浓度表示的平衡常数,气体分压=气体的体积分数×体系总压)。
(2)利用乙醇重整制氢是获得氢能的研究热点,其主要反应原理为:
反应Ⅰ: ![]() H1
H1
若同时通入水蒸汽,还会发生如下反应
反应Ⅱ:![]() H2
H2
反应Ⅲ:![]() H3
H3
反应Ⅳ:![]() H4
H4
一定温度下,某恒压密闭容器中充入一定量的![]() 发生反应。
发生反应。
已知:氢气选择性指转化的原料气中,转化成氢气的氢元素质量与转化的氢元素总质量的比值。
①下列有关说法正确的是_______________。
A.当混合气的平均相对分子质量不变时,说明反应达到平衡状态
B.增大乙醇初始浓度,能够提高乙醇的平衡转化率
C.其它条件不变,掺入稀有气体,可提高乙醇平衡转化率
D.其它条件不变,掺入水蒸气,可提高氢气的选择性和氢气的体积分数
②下图为上述条件下n(H2)随反应时间的变化曲线图。若其它初始条件相同,只把容器变为恒容密闭容器,请画出恒容条件下,n(H2)随反应时间的变化曲线图________________。
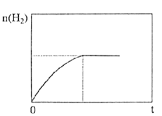
③乙醇重整制氢过程中,还可能生成固态炭,固态炭的生成会造成催化剂失活,应尽量避免。研究其它条件相同下,反应温度、氧醇比、水醇比与生成固态炭的条件,得到下图:
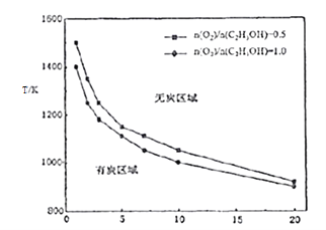
试根据图象分析,反应温度、氧醇比、水醇比对固态炭生成的影响_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:2X(g)+Y(g) ![]() 2Z(g) △H<0,下图是表示该反应速率(v)随时间(t)变化的关系图。t1、t2、t5时刻外界条件均有改变(但都没有改变各物质的用量)。则下列说法中正确的是( )
2Z(g) △H<0,下图是表示该反应速率(v)随时间(t)变化的关系图。t1、t2、t5时刻外界条件均有改变(但都没有改变各物质的用量)。则下列说法中正确的是( )

A. t3时降低了温度 B. t5时增大了压强
C. t6时刻后反应物的转化率最低 D. t4时该反应的平衡常数小于t6时反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一种形状酷似罗马两面神Janus的有机物结构简式,化学家建议将该分子叫做“Janusene”,下列说法正确的是
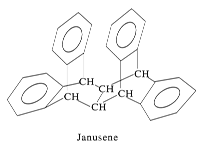
A.Janusene的分子式为C30H20
B.Janusene属于苯的同系物
C.Janusene苯环上的一氯代物有8种
D.Janusene既可发生氧化反应,又可发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、101kPa条件下,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5kJ/mol、285.8kJ/mol、870.3kJ/mol,则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S是一种剧毒气体,工业生产中可以通过多种手段对其进行回收或再利用。
Ⅰ.900℃时可以用克劳斯法回收H2S气体,该过程中涉及的部分反应如下:
①2H2S(g)+O2(g)![]() S2(g)+2H2O(g) △H=-316.8kJmol-1
S2(g)+2H2O(g) △H=-316.8kJmol-1
②2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) △H=-1040.2kJmol-1
(1)4H2S(g)+2SO2(g)![]() 3S2(g)+4H2O(g)的△H=___
3S2(g)+4H2O(g)的△H=___
(2)若在900℃以上绝热、恒容的密闭容器中,投入一定量的H2S、O2发生反应①,下列说法能说明反应达到平衡状态的是___
a.混合气体密度不随时间变化而变化
b.v正(O2)=2v逆(H2O)
c.体系压强不随时间变化而变化
d.反应体系温度不变
e.混合气体平均相对分子质量不变
f.单位时间内生成nmolS2,同时生成2nmolH2S
Ⅱ.工业上还可以通过硫化氢分解对其进行处理、利用:2H2S(g)![]() S2(g)+2H2(g),在2.0L恒容密闭容器中充入0.1molH2S,不同温度下测得H2S的转化率与时间的关系如图1所示:
S2(g)+2H2(g),在2.0L恒容密闭容器中充入0.1molH2S,不同温度下测得H2S的转化率与时间的关系如图1所示:
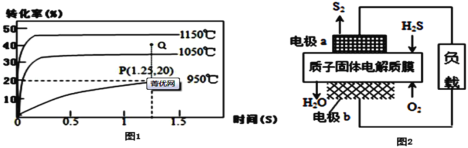
(3)950℃时,0~1.25s生成S2(g)的平均反应速率为___
(4)该反应的△H___0(填“>”“<”或“=”),1050℃达到平衡时H2S的转化率为35%,则该温度下,平衡常数K=___(保留一位有效数字),该温度下Q点时反应___(填“正向移动”“逆向移动”或“不移动”)
Ⅲ.对H2S废气进行利用的另一种途径是将其设计成质子膜—H2S燃料电池,反应原理为2H2S(g)+O2(g)═S2(s)+2H2O(l)。电池结构示意图如图2:
(5)电极a上发生的电极反应式为___。
(6)设NA为阿伏伽德罗常数的值,当电路中通过3mol电子时,通过质子膜进入___(填“正极区”或“负极区”)的H+数目为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com