
【题目】磷在氧气中燃烧,可能生成P2O3和P2O5 , 已知单质磷(P)的燃烧热为X kJ/mol,0.1molP在2.24L O2(标准状况下)燃烧至反应物耗尽时,放出Y kJ 的热量,则下列说法错误的是( )
A.生成0.025 mol P2O5
B.生成 P2O3所释放的热量为(Y﹣0.05X) kJ
C.2P(s)+ ![]() O2(g)=P2O3(s)△H=﹣(40Y﹣2X)kJ?mol﹣1
O2(g)=P2O3(s)△H=﹣(40Y﹣2X)kJ?mol﹣1
D.生成的 P2O3与 P2O5的质量之比为 1:1
【答案】D
【解析】解:A、根据以上分析,0.1molP在2.24L O2(标准状况下)燃烧至反应物耗尽,故P原子与O原子的数目之比为0.1mol: ![]() mol×2=1:2,2:5<1:2<2:3,故反应产物为P2O3、P2O5 , 故A正确;B、根据以上分析,生成P2O3的物质的量为0.025mol,生成P2O5的物质的量为0.025mol,又单质磷(P)的燃烧热为X kJ/mol,所以生成 P2O3所释放的热量为(Y﹣0.05X) kJ,故B正确;
mol×2=1:2,2:5<1:2<2:3,故反应产物为P2O3、P2O5 , 故A正确;B、根据以上分析,生成P2O3的物质的量为0.025mol,生成P2O5的物质的量为0.025mol,又单质磷(P)的燃烧热为X kJ/mol,所以生成 P2O3所释放的热量为(Y﹣0.05X) kJ,故B正确;
C、由B得出,生成P2O3的物质的量为0.025mol,释放的热量为(Y﹣0.05X) kJ,所以2P(s)+ ![]() O2(g)=P2O3(s)△H=﹣(40Y﹣2X)kJmol﹣1 , 故C正确;
O2(g)=P2O3(s)△H=﹣(40Y﹣2X)kJmol﹣1 , 故C正确;
D、根据以上分析,生成的 P2O3与 P2O5的质量之比为2.75g:3.55g,故D错误;
故选:D.
【考点精析】认真审题,首先需要了解燃烧热(在101kPa时1mol H2物质完全燃烧生成稳定的氧化物时所放出的能量,叫该物质的燃烧热).


科目:高中化学 来源: 题型:
【题目】合成氨的热化学方程式为N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJ/mol.现将1molN2(g)、3molH2(g)充入一容积为2L的密闭容器中,在500℃下进行反应,10min时达到平衡,NH3的体积分数为φ,下列说法中正确的是( ) 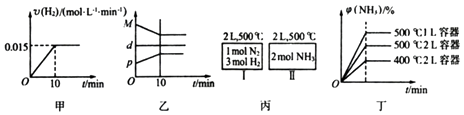
A.若达到平衡时,测得体系放出9.24kJ热量,则H2反应速率变化曲线如图甲所示
B.反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为p,三者关系如图乙
C.如图丙所示,容器I和II达到平衡时,NH3的体积分数为φ,则容器I放出热量与容器II吸收热量之和为92.4kJ
D.若起始加入物料为1 mol N2 , 3 mol H2 , 在不同条件下达到平衡时,NH3的体积分数变化如图丁所示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:W、Y、Z、T、M为前四周期元素,且原子半径依次增大.请填空:
(1)W,Z是形成化合物种类最多的两种元素,写出Z原子的核外电子排布图;
(2)化合物YW3极易溶于水的原因;YW3的分子构型为 . YW3属于(填“极性”或“非极性”)分子,其中Y的化合价为 .
(3)元素T的原子中电子共占据了7个轨道,则T在元素周期表周期族.T的化合物TY熔融时不导电,常用作砂轮及耐高温材料,由此推知,它属于(填编号字母);
a.离子晶体 b.原子晶体 c.分子晶体 d.无法判断
(4)M3+的3d轨道为半充满,则M的原子的电子排布式为 , M位于周期表的区(按电子的填入顺序划分),M的晶体中的粒子采用的是体心立方堆积,则该种堆积方式的配位数为 , 若其晶胞的边长为acm,M的摩尔质量为Mr g/mol,阿伏加德罗常数的值为NA , 则其密度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 医用酒精的浓度通常是95%
B. 蛋白质是结构复杂的高分子化合物,分子中都含有C、H、O、N四种元素
C. 淀粉、纤维素和油脂都属于天然高分子化合物
D. 合成纤维和光导纤维都是新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋是重要的调味品,我国劳动人民在很早以前就知道酒在空气中能“酸败成醋”,该事实的实质是
A. 酒中的乙醇挥发,使乙醇的含量降低B. 酒中的杂质腐败成酸
C. 酒中的乙醇被氧化成乙醛D. 酒中的乙醇被氧化成乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由中学化学常见元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有下图所示转化关系,A是由地壳中含量最多的金属元素组成的。请回答:
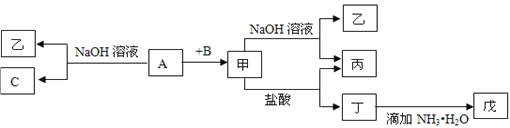
(1)写出下列物质的化学式:乙_______、丁_______、戊_______。
(2)写出甲物质在工业上的一种主要用途:______________________________。
(3)写出甲→乙+丙反应的离子方程式:______________________________________;
丁→戊反应的离子方程式:___________________________________________;
A→乙+C反应的化学方程式_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列实验需要在哪套装置中进行:(填序号,每套装置仅使用一次)
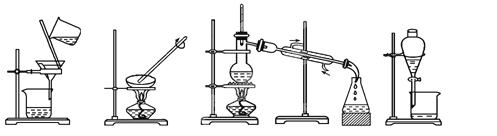
① ② ③ ④
从海水中提取水:____________;从KCl溶液中获取KCl晶体:____________;
分离CaCO3和水:____________;分离植物油和水:____________。
(2)现有甲、乙两瓶无色溶液,已知它们可能为AlCl3溶液和NaOH溶液。现分别将一定体积的甲、乙两溶液混合,具体情况如下表所示,请回答:
实验① | 实验② | 实验③ | |
取甲瓶溶液的量 | 400 mL | 120 mL | 120 mL |
取乙瓶溶液的量 | 120 mL | 440 mL | 400 mL |
生成沉淀的量 | 1.56 g | 1.56 g | 3.12 g |
①甲瓶溶液为________溶液。
②乙瓶溶液为________溶液,其物质的量浓度为________mol·L-1。
【答案】 ③ ② ① ④ AlCl3 NaOH 0.5
【解析】(1)水易挥发,海水中提取水可用蒸馏的方法,答案选③;从 KCl溶液中获取KCl晶体,可用蒸发的方法,答案选②;CaCO3不溶于水,分离CaCO3和水,可用过滤的方法,答案选①;植物油和水互不相溶,分离植物油和水,可用分液的方法,答案选④;
(2)氯化铝滴入NaOH溶液中,开始氢氧化钠过量,发生反应AlCl3+4NaOH═NaAlO2+3NaCl+2H2O,然后发生反应:3NaAlO2+AlCl3+6H2O=4Al(OH)3↓+3NaCl;氢氧化钠溶液滴入AlCl3溶液中,开始发生反应:AlCl3+3NaOH═Al(OH)3↓+3NaCl,然后发生反应:Al(OH)3+NaOH═NaAlO2+2H2O,由②和③可知,一定量的甲与乙反应时,乙的量越多,生成的沉淀越少,则乙为NaOH溶液,即甲为AlCl3溶液,乙为NaOH溶液,由实验①②可知,实验①中NaOH不足,AlCl3有剩余,根据AlCl3+3NaOH═Al(OH)3↓+3NaCl,1.56g沉淀的物质的量为![]() =0.02mol,则NaOH的物质的量为0.02mol×3=0.06mol,故NaOH溶液的物质的量浓度为0.06mol/0.12L=0.5mol/L。
=0.02mol,则NaOH的物质的量为0.02mol×3=0.06mol,故NaOH溶液的物质的量浓度为0.06mol/0.12L=0.5mol/L。
【题型】综合题
【结束】
18
【题目】(1)向AlCl3溶液中,滴加少量NaOH溶液,现象是________________________
继续滴加NaOH溶液至过量,现象是_______________。
(2)钠与水反应的离子方程式为_______________,该反应中氧化剂是_______________,产生1mol H2时,转移电子的物质的量为_______________mol。
(3)经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O
①该反应的氧化剂是_______,被氧化的是_________元素。
②若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中碘元素的检验可经过以下四个步骤完成(已知H2O2在酸性条件下能将海带中的I氧化成I2 , I2遇淀粉变蓝),各步骤中选用的实验用品不正确的是( ) 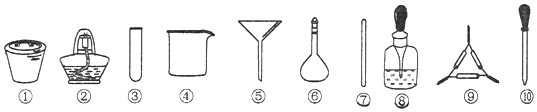
A.将海带剪碎后灼烧成灰,选用①、②和⑨
B.将海带灰加蒸馏水溶解,选用④、⑥和⑦
C.过滤得到滤液,选用④、⑤和⑦
D.取滤液,先加入几滴稀硫酸,再滴加H2O2 , 最后滴加淀粉溶液,选用③和⑩
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com