
世界卫生组织(WHO)将二氧化氯(ClO2)列为A级高效、安全灭菌消毒剂,ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,它在食品保鲜、饮用水消毒等方面有着广泛的应用。
(1)实验室制备ClO2的方法之一为:
2KClO3+H2C2O4+H2SO4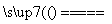 2ClO2↑+K2SO4+2CO2↑+2H2O(H2C2O4俗称草酸,其中H为+1价,O为-2价)则下列说法正确的是________。
2ClO2↑+K2SO4+2CO2↑+2H2O(H2C2O4俗称草酸,其中H为+1价,O为-2价)则下列说法正确的是________。
A.KClO3在反应中得到电子
B.ClO2是氧化产物
C.H2C2O4在反应中被氧化
D.1 mol KClO3参加反应有2 mol电子转移
(2)KClO3和浓盐酸在一定温度下反应也会生成绿黄色的二氧化氯。其变化可表示为2KClO3+4HCl(浓)===2KCl+2ClO2↑+Cl2↑+2H2O
①浓盐酸在反应中表现出来的性质是__________________________________________;
②已知每产生0.1 mol Cl2,则发生转移的电子的物质的量为0.2 mol。ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒后的还原产物是氯离子,则其消毒的效率(以单位质量得到的电子数表示)是Cl2的________倍。
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
工业废水中常含有一定量的Cr2O72﹣和CrO42﹣,它们会对人类及生态系统产生很大损害,必须进行处理.常用的处理方法有两种.
方法1:还原沉淀法该法的工艺流程为:CrO42﹣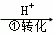 Cr2O72﹣
Cr2O72﹣ Cr3+
Cr3+ Cr(OH)3↓其中第①步存在平衡:2CrO42﹣(黄色)+2H+⇌Cr2O72﹣(橙色)+H2O
Cr(OH)3↓其中第①步存在平衡:2CrO42﹣(黄色)+2H+⇌Cr2O72﹣(橙色)+H2O
(1)若平衡体系的pH=2,该溶液显 橙 色.
(2)能说明第①步反应达平衡状态的是 c .
a.Cr2O72﹣和CrO42﹣的浓度相同 b.2v(Cr2O72﹣)=v(CrO42﹣) c.溶液的颜色不变
(3)第②步中,还原1molCr2O72﹣离子,需要 6 mol的FeSO4•7H2O.
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH﹣(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)•c3(OH﹣)=10﹣32,要使c(Cr3+)降至10﹣5mol/L,溶液的pH应调至 5 .
方法2:电解法,该法用Fe做电极电解含Cr2O72﹣的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
(5)用Fe做电极的原因为 阳极反应为Fe﹣2e﹣═Fe2+,提供还原剂Fe2+ .
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 2H++2e﹣═H2↑ ,溶液中同时生成的沉淀还有 Fe(OH)3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
A.铝投入氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑
B.氯气与水反应:Cl2 + H2O = 2H+ + Cl- + ClO -
C.碳酸氢钠溶液与少量石灰水反应:2HCO3- + Ca2+ + 2OH- = CaCO3↓+ CO32- + 2H2O
D.单质铜与稀硝酸反应:Cu +2H+ +2NO3- = Cu2+ + 2NO↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在25℃时,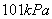 条件下,将
条件下,将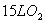 通入10LCO和
通入10LCO和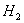 的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和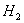 的混合气中V(CO)=__________L,
的混合气中V(CO)=__________L,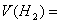 ___________L。
___________L。
(2)若剩余气体的体积是aL,则原CO和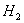 的混合气中
的混合气中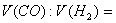 _________。
_________。
(3)若剩余气体的体积是aL,则a的取值范围是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铁单质及其化合物在生产、生活中应用广泛.请回答下列问题:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应式为
________________________________________________________________________.
(2)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是________________________________________________________________________.
(3)硫酸铁可作絮凝剂,常用于净水,其原理是_______________________________
_________________________________________________________(用离子方程式表示).
在使用时发现硫酸铁不能使酸性废水中的悬浮物沉降而除去,其原因是_____________
________________________________________________________________________.
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO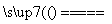 3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是____________.
3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是____________.
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母).
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁的表面能形成致密的氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
我国将协同世界各经济体共同应对温室效应对地球的挑战.造成温室效应的主要原因是人类向空气大量排放了( )
|
| A. | CO | B. | SO2 | C. | CO2 | D. | NO |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列家庭化学小实验不能达到预期目的是( )
|
| A. | 用米汤检验食用加碘盐(含KIO3)中含有碘 |
|
| B. | 用醋、石灰水验证蛋壳中含有碳酸盐 |
|
| C. | 用碘酒检验汽油中是否含有不饱和烃 |
|
| D. | 用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
材料是人类赖以生存的重要物质基础.
(1)合金是被广泛应用的金属材料.
①下列有关合金性质的说法正确的是 (填字母).
a.合金的熔点一般比它的成分金属高
b.合金的硬度一般比它的成分金属高
c.组成合金的元素种类相同,合金的性能就一定相同
②钢属于 (填“铁合金”或“铝合金”).
③铁锈蚀主要发生的是电化学腐蚀,其负极反应式为 F + .
(2)传统无机非金属材料包括玻璃、水泥和 陶瓷 .生产玻璃发生的化学反应方程式: 、 .
(3)合成塑料、合成橡胶和 合成纤维 是常说的三大合成材料.下列属于塑料制品的是 (填字母).
a.汽车轮胎 b.玻璃钢 c.聚乙烯制品.
查看答案和解析>>
科目:高中化学 来源: 题型:
化学工作者从有机反应RH+Cl2(g)===RCl(l)+HCl(g)中受到启发,提出的在农药和有机合成工业中可获得副产品盐酸的设想已成为现实。试指出从上述反应产物中分离得到盐酸的最佳方法是(g表示物质为气态,l表示物质为液态。HCl极易溶于水,得到盐酸;有机物一般难溶于水)( )
A.蒸馏法 B.水洗分液法 C.升华法 D.有机溶剂萃取法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com