
�� ��1����Ũ��������250mL2mol∙L-1������Һʱ������������������ձ����������ͽ�ͷ�ι�֮�⣬����Ҫ �����������ƣ������������ƹ���ʾ��ͼ�У��д�����ǣ���д��ţ� ��
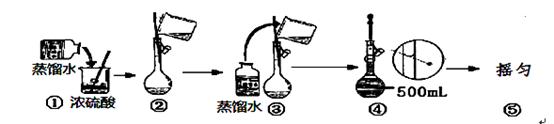
 ��2����Ҫ������ƿ����500mL0.4mol∙L-1Na2CO3��Һ,��õ���Һ������
��2����Ҫ������ƿ����500mL0.4mol∙L-1Na2CO3��Һ,��õ���Һ������
��ƿ����Ҫ���ϱ�ǩ�������������ͼ��ǩ�ϵ���������ȥ��
��3�����������ʹ������Һ�����ʵ���Ũ��ƫ�͵��� ������ţ�
A. ����ƿ������ˮϴ����,δ���������������
B. NaOH�ܽ�������������ƿ��
C. ����ʱ,���ӿ̶��� D. ҡ�Ⱥ���Һ��δ���̶���,������ˮ���̶���
 �� ij��ѧС��ģ�⡰�����Ƽ������NaCl��NH3��CO2��ˮ��Ϊԭ���Լ���
�� ij��ѧС��ģ�⡰�����Ƽ������NaCl��NH3��CO2��ˮ��Ϊԭ���Լ���
ͼ��ʾװ����ȡNaHCO3����Ӧ�Ļ�ѧ����ʽΪNH3+CO2+H2O+NaCl = NaHCO3��+NH4Cl��
Ȼ���ٽ�NaHCO3�Ƴ�Na2CO3��
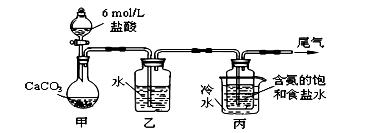
�� װ���ҵ������� ��Ϊ��ֹ��Ⱦ��
����β���к��е� ��Ҫ�������մ�����
����װ�ñ��в�����NaHCO3��ȡNa2CO3ʱ����Ҫ���е�ʵ������� ��
�� ��NaHCO3ת��ΪNa2CO3�Ļ�ѧ����ʽΪ ��
 ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NAΪ�����ӵ�������ֵ������������ȷ����
A��25�棬pH��2��HCl��Һ�к���H������ĿΪ0.01NA
B��1mol Na2O2�����к��е�������������Ϊ4 NA
C�����³�ѹ�£�14g��ϩ�ͻ�����Ļ�����У�����̼ԭ�ӵ���ĿΪNA
D����״���£�2.24LCl2��������NaOH��Һ��Ӧ��ת�Ƶĵ�����ĿΪ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�£�N2H4��������ȼ�ϵ����һ�ֻ�������ȼ�ϵ�أ���������Һ��20%��30%��KOH��Һ������ܷ�ӦΪ��N2H4��O2��N2����2H2O�����й��ڸ�ȼ�ϵ�ع���ʱ��˵����ȷ����( )
A.��ع���ʱ������������Һ�ļ�����ǿ
B.�����ĵ缫��Ӧʽ�ǣ�O2��4H+��4e����2H2O
C.�����ĵ缫��Ӧʽ��:N2H4��4OH�D�D4e����4H2O��N2��
D.��Һ���������������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Na2CO3��NaHCO3���ʵ�˵������ȷ���ǣ� ��
A�����ȶ��ԣ�NaHCO3 �� Na2CO3
B�������ʯ��ˮ��Ӧ��Na2CO3��NaHCO3��Һ�о��г�������
C����ͬ�¶�ʱ����ˮ�е��ܽ��ԣ�NaHCO3 �� Na2CO3
D����������NaHCO3��Na2CO3�ֱ����������ᷴӦ����ͬ��ͬѹ�£����ɵ�CO2�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���г�ȥ���ʵķ�����ȷ���ǣ� ��
| ���� | ���� | �Լ� | ��Ҫ���� | |
| A | NaHCO3���� | Na2CO3���� | / | ���� |
| B | SiO2 | Fe2O3 | ���� | ���� |
| C | KBr��Һ | Br2 | KOH��Һ | ��Һ |
| D | Cl2 | HCl | ����̼������Һ | ϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и�������ʾ��ͼһ�µ���
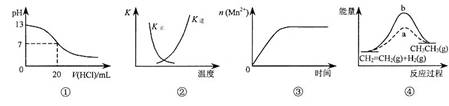
A��ͼ�ٱ�ʾ25��ʱ����0.1 mol��L��1����ζ�20 mL 0.1 mol��L��1 NaOH��Һ����Һ��pH�����������ı仯
B��ͼ�������߱�ʾ��Ӧ2SO2(g) + O2(g) 2SO3(g) ��H < 0 �����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯
2SO3(g) ��H < 0 �����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯
C��ͼ�۱�ʾ10 mL 0.01 mol��L��1 KMnO4 ������Һ�������0.1 mol��L��1 H2C2O4��Һ���ʱ��n(Mn2+) ��ʱ��ı仯
D��ͼ����a��b���߷ֱ��ʾ��ӦCH2��CH2 (g) + H2(g) CH3CH3(g)����H< 0ʹ�ú�δʹ�ô���ʱ����Ӧ�����е������仯
CH3CH3(g)����H< 0ʹ�ú�δʹ�ô���ʱ����Ӧ�����е������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����״̬�£�Na�ĵ��ʺ�FeCl2����ɿɳ����(װ��ʾ��ͼ����)����Ӧԭ��Ϊ��
2Na+ FeCl2 Fe+ 2NaCl
Fe+ 2NaCl
�ŵ�ʱ����ص�������ӦʽΪ �����ʱ�� (д��������)�缫�ӵ�Դ�ĸ������õ�صĵ����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ����
A��pH=9��NaHA��Һ��c(Na+)>c(HA��)>c(A2��)>c(H2A)
B��Na2CO3��Һ��c(H+)��c(OH��) = c(HCO3��) +2c(CO32��)��c(Na+)
C��ϡ�����м���һ������ˮ����Һ�Լ��ԣ�c(NH4+)>c(Cl��)>c(OH��)>c(H+)
D����0.1mol��L��1 HF��Һ��0.1mol��L��1 KF��Һ��������:c(F��)+c(HF)=0.2mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ԭ�ƻ�ʵ��ȫ������ͨѶ�跢��77������,��һ������ҿ(Ir)Ԫ�ص�ԭ�Ӻ��������ǡ�����,��˳�Ϊ��ҿ�Ǽƻ���.��֪ҿ��һ��ͬλ�ص�������Ϊ191,������ڵ���������������֮����
A. 77 B. 114 C. 37 D. 268
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com