
恒温恒容下,向2 L密闭容器中加入MgSO4(s)和CO(g),发生反应:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g)
MgO(s)+CO2(g)+SO2(g)
反应过程中测定的部分数据见下表:
反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(SO2) / mol |
0 | 2.0 | 2.0 | 0 |
2 | 0.8 | ||
4 | 1.2 | ||
6 | 1.2 | 2.8 |
下列说法正确的是
A.0~2 min内的平均速率为υ (CO)=0.6 mol/(L·min)
B.4 min后,平衡移动的原因可能是向容器中加入了2.0 mol的SO2
C.4 min后,若升高温度,SO2物质的量浓度变为0.7mol/L,则正反应为放热反应
D.其他条件不变,若起始时容器中MgSO4、CO均为1.0 mol,则平衡时n(SO2)=0.6 mol
科目:高中化学 来源:2016届贵州省兴义市高三上学期期中测试理综化学试卷(解析版) 题型:选择题
下列离子方程式正确的是:
A.过量氯气通入溴化亚铁溶液中:Fe2++2Br-+2Cl2=Fe3++Br2+4Cl-
B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O
C.碳酸氢钙和过量的氢氧化钠溶液反应:Ca2++ OH—+HCO3—=CaCO3↓+ H2O
D.用FeCl3溶液腐蚀印刷电路板:Cu+Fe3+=Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源:2016届河北省邯郸市高三上学期10月月考化学试卷(解析版) 题型:填空题
下图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:

(1)表中某元素最高正价氧化物的水化物与其氢化物之间能相互反应生成离子化合物,则该离子化合物的名称是______,由元素④、⑥、⑦、⑧形成的简单离子的半径由大到小的顺序是_______(用离子符号表示,下同)。②、④、⑤元素的氢化物的沸点由高到低的顺序是____________。
(2)分别由上述两种元素组成、均为10e-的阴、阳离子,在加热条件下反应生成两种10e-的分子,写出该离子反应方程是________________。
(3)由表中四种元素形成X、Y、Z、M、N等常见物质,X、Y含有一种相同元素,其中X焰色反应呈黄色,可发生以下反应:
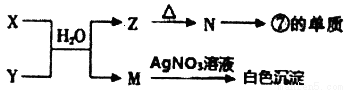
① X、Y与水混合后反应的离子方程式为________________。
② N→⑦的单质反应的化学方程式为_________________。
③ 元素④形成的单质的电子式为________________。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期开学联考化学试卷(解析版) 题型:实验题
三草酸合铁酸钾晶体K3[Fe(C2O4)3]?3H2O可用于摄影和蓝色印刷.某小组将无水三草酸合铁酸钾在一定条件下加热分解,对所得气体产物和固体产物进行实验和探究.请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程.
限选试剂:浓硫酸、1.0mol•L﹣1HNO3、1.0mol•L﹣1盐酸、1.0mol•L﹣1NaOH、3%H2O2、0.1mol•L﹣1KI、0.1mol•L﹣1CuSO4、20%KSCN、澄清石灰水、氧化铜、蒸馏水.
(1)该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3.通过 可验证固体产物中是否含有钾元素.
(2)固体产物中铁元素存在形式的探究.
①提出合理假设:
假设1:全部是铁单质;
假设2: ;
假设3: .
②设计实验方案证明你的假设
③实验过程
根据②中方案进行实验.在写出实验步骤、预期现象与结论.

查看答案和解析>>
科目:高中化学 来源:2016届福建省四地六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
碘是一种与人的生命活动密切相关的元素,已知I2能溶于NaOH或KI溶液,反应方程式分别为:3I2+6OH﹣═5I﹣+IO3-+3H2O(HIO不稳定,易发生歧化反应)和I2+I﹣═I3-,溴化碘(IBr)是一种卤素互化物,具有与卤素单质相似的性质,下列反应方程式中不正确的是
A.IBr加入Na2S溶液中产生黄色浑浊:IBr+S2﹣═I﹣+Br﹣+S↓
B.IBr加入KI溶液中:IBr+2I﹣═Br﹣+ I3-
C.IBr加入NaOH溶液中:IBr+2OH﹣═BrO﹣+I﹣+H2O
D.IBr加入AgNO3溶液中:3IBr+5Ag++3H2O═3AgBr↓+2AgI↓+ IO3-+6H+
查看答案和解析>>
科目:高中化学 来源:2016届江西省吉安市高三上学期第一次月考化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值 下列说法正确的是
A.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA
B.标准状况下,11.2L的戊烷所含的分子数为0.5NA
C.标准状况下,2.24 L Cl2溶于水中达到饱和,转移的电子数是0.1NA
D.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH﹣数目为0.2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省西安市高一上10月月考化学试卷(解析版) 题型:填空题
(18分)(1)标准状况下,67.2L CO2约是___________ mol,约含有___________个CO2 分子,其中约含有___________ mol氧原子。
(2)要得到含溶质0.2mol的溶液,需取0.05mol/L的氢氧化钡溶液___________mL。
(3)9.2g氮的氧化物NOx中含有N原子数为0.2mol,则NOx的摩尔质量为__________,x的数值为___________,这些质量的NOx在标准状况下的体积约为_____________L。
(4)常温下,相对分子质量为M的某无水盐A的溶解度为Sg,则常温时,该盐饱和溶液质量分数为__________,如果已知该饱和溶液的密度为ρg/cm3,则该溶液的物质的量浓度为___________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上期中考试化学试卷(解析版) 题型:填空题
(6分)I. (1)在Al2(SO4)3和MgSO4组成的混合物中,Al3+与Mg2+的物质的量之比为2∶3,则在含有4 mol SO42-的混合物中,MgSO4的质量是______________克。
(2)V ml Al2(SO4)3溶液中含有Al3+ a g,取V/4 ml溶液稀释到4V ml,则稀释后溶液中SO42-的物质的量浓度是______________ mol/L。
II.在120 ℃时分别进行如下四个反应:
A.2H2S (g) + O2 (g) ==2H2O (g)+2S (s) B.2H2S (g)+3O2 (g)==2H2O (g)+2SO2 (g)
C.C2H4 (g)+3O2 (g)==2H2O (g)+2CO2 (g) D.C4H8 (g)+6O2 (g)==4H2O (g)+4CO2 (g)
(1)若反应在容积固定的容器内进行,反应前后气体密度(d)和气体总压强(p)分别符合关系式d前=d后和p前>p后的是__________;符合关系式d前=d后和p前=p后的是__________。(请填写反应的代号)
(2)若反应在压强恒定容积可变的容器内进行,反应前后气体密度(d)和气体体积(V)分别符合关系式d前>d后和V前<V后的是________;符合d前>d后和V前>V后的是________。(请填写反应的代号)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南信阳高级中学高二开学考试化学试卷(解析版) 题型:选择题
下列大小比较正确的是
A.稳定性:HI>HBr>HCl>HF B.元素非金属性:Si>P>S>Cl
C.沸点: 正丁烷>异丁烷>丙烷 D.碱性NaOH>KOH>Ca(OH)2>Ba(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com