
����һ�����˵������������ص�Ԫ�أ���֪I2������NaOH��KI��Һ����Ӧ����ʽ�ֱ�Ϊ��3I2+6OH���T5I��+IO3-+3H2O��HIO���ȶ��������绯��Ӧ����I2+I���TI3-���廯�⣨IBr����һ��±�ػ����������±�ص������Ƶ����ʣ����з�Ӧ����ʽ�в���ȷ����
A��IBr����Na2S��Һ�в�����ɫ���ǣ�IBr+S2���TI��+Br��+S��
B��IBr����KI��Һ�У�IBr+2I���TBr��+ I3-
C��IBr����NaOH��Һ�У�IBr+2OH���TBrO��+I��+H2O
D��IBr����AgNO3��Һ�У�3IBr+5Ag++3H2O�T3AgBr��+2AgI��+ IO3-+6H+
 ���100��1�ž�ϵ�д�
���100��1�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ������ѧ�ڶ���ģ��������ۻ�ѧ�Ծ��������棩 ���ͣ������
����ѧһһѡ��5���л���ѧ��������15�֣�
ijҩ���ͨ�����·����ϳɣ�

ע����ŵ�����һ���������ʪ�Թؽ���ҩ���ش��������⣺
��1����ŵ����еĺ���������Ϊ �� �������ƣ���
��2����Ӧ���м�����Լ�X�ķ���ʽΪC8H8O2��X�Ľṹ��ʽΪ ��
��3���������岽��Ӧ�У�����ȡ����Ӧ���� ������ţ���
��4��B��һ��ͬ���칹����������������
���ܷ���������Ӧ����ˮ�����֮һ����FeCl3��Һ������ɫ��Ӧ��
��������6�ֲ�ͬ��ѧ�������⣬�ҷ����к�������������
д����ͬ���칹��Ľṹ��ʽ�� ��
��5����������֪ʶ����������Ϣ��д����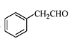 Ϊԭ���Ʊ�
Ϊԭ���Ʊ�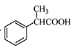 �ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
���к͵ζ����ⶨ�ռ�Ĵ��ȣ��ռ��е����ʲ����ᷴӦ���������ʵ��ش�
��1���������õ�8.8g�ռ���Ʒ���Ƴ�500mL����Һ�����ƹ���ʹ�õ���Ҫ������500mL����ƿ����Ͳ���ձ�����ͷ�ι��⣬����һ�ֱ���ʹ�õ�������___________��
��2����_______ʽ�ζ�����ȡ10.00mL����Һ����ƿ�У����뼸�η�̪��
��3����0.20mol•L-1�ı�����ζ�����Һ���жϵζ��յ�������ǣ�_________��
��4�����ʵ�������ȷ���ӵζ���ʼ����������Һ�е�����Ũ�ȹ�ϵ���Գ��ֵ���_______�������ĸ��ţ�
A��c��Na+����c��Cl������c��H������c��OH����
B��c��Na+����c��OH������c��Cl������c��H����
C��c��Na+��+c��H����=c��OH����+c��Cl����
D��c��Cl����+c��Na+����c��OH����+c��H����
��5�������������ݼ��㣬c��NaOH��_______mol/L���ռ�Ĵ���Ϊ________%������������
�ζ����� | ����Һ�����mL�� | �����������mL�� | |
�ζ�ǰ������mL�� | �ζ��������mL�� | ||
��һ�� | 10.00 | 0.60 | 20.50 |
�ڶ��� | 10.00 | 3.00 | 23.10 |
��6�������������֣�����ʵ��IJⶨ������ռ��ʵ�ʴ���ƫ�ߣ�������Ŀ���ԭ����_________�������ĸ��ţ���ѡ����Ϊ0�֣�
A���ζ�ǰƽ�ӣ��ζ�����
B��δ�ñ�Һ��ϴ�ζ���
C���ô���Һ��ϴ��ƿ
D����С�Ľ���Һ������ƿ����
E���ζ��ӽ��յ�ʱ������������ˮ��ϴ��ƿ�ڱ�
F���ζ�ǰ���������ݣ��ζ�����ʧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡУ������ѧ�ڽ��Կ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȷ��ʾ���з�Ӧ�����ӷ���ʽ����
A����������ͭ��Һ��Ӧ��Al+Cu2+=Al3++Cu
B��̼�ᱵ����ϡ���CO32-+2H+=H2O+CO2��
C������ϡ���ᷴӦ��Fe+2H+=Fe3++H2��
D�������ˮ����2CH3COOH+CaCO3=2CH3COO-+Ca2++CO2��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ������ѧ�ڿ�ѧ������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йص������Һ��˵����ȷ����
A��Na2SO3��Һ��ˮϡ�ͺ�pH��KW����С
B��0.1mol•L��1Na2CO3��Һ�У�c��OH����=c��H+��+c��HCO3����+2c��H2CO3��
C��Ũ�ȷֱ�Ϊ0.2mol•L��1��0.1mol•L��1��CH3COOH��Һ�У�c��H+��֮�ȵ���2��1
D�������£�PH=12�İ�ˮ��PH=2��H2SO4��Һ�������Ϻ���Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ������ѧ�ڵ�һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���º����£���2 L�ܱ������м���MgSO4��s����CO��g����������Ӧ��
MgSO4��s��+CO��g�� MgO��s��+CO2��g��+SO2��g��
MgO��s��+CO2��g��+SO2��g��
��Ӧ�����вⶨ�IJ������ݼ��±���
��Ӧʱ��/min | n��MgSO4��/mol | n��CO��/mol | n��SO2�� / mol |
0 | 2.0 | 2.0 | 0 |
2 | 0.8 | ||
4 | 1.2 | ||
6 | 1.2 | 2.8 |
����˵����ȷ����
A��0��2 min�ڵ�ƽ������Ϊ�� ��CO����0.6 mol/��L��min��
B��4 min��ƽ���ƶ���ԭ��������������м�����2.0 mol��SO2
C��4 min���������¶ȣ�SO2���ʵ���Ũ�ȱ�Ϊ0.7mol/L��������ӦΪ���ȷ�Ӧ
D�������������䣬����ʼʱ������MgSO4��CO��Ϊ1.0 mol����ƽ��ʱn��SO2��=0.6 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
��10�֣�
��1�������£�0.05mol/L������Һ�У�c��H+��= mol/L��pHֵΪ ��ˮ�����c��H+��= mol/L��
��2��ij�¶ȣ���ˮ��c��H+��=3��10-7mol/L����ˮ��c��OH-��= mol/L����ʱ��ˮ����ϡ������c��H+��Ϊ1��10-5mol/L���ʱc��OH-��= mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶������п��Ի�ѧ�Ծ��������棩 ���ͣ������
��ÿ��2�֣���10�֣���Ԫ������Ҫ�Ľ���Ԫ�أ��������ڹ�ҵ��������ʹ�õ���Ϊ�㷺�������кܶ���Ҫ�Ļ����P�仯ѧ��Ӧ��
������ˮ��Ӧ��3Fe��s����4H2O��g����Fe3O4��s����4H2��g�� ��H
��1��������Ӧ��ƽ�ⳣ������ʽK��_____________��
��2����֪����3Fe��s����2O2��g����Fe3O4��s�� ��H1����1118.4kJ��mol��1
��2H2��g����O2��g����2H2O��g�� ��H2����483.8 kJ��mol��1
��2H2��g����O2��g����2H2O��l�� ��H3����571.8 kJ��mol��1
���H��_____________��
��3����t��ʱ���÷�Ӧ��ƽ�ⳣ��K��16����2L���º����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⡣
Fe | H2O��g�� | Fe3O4 | H2 | |
��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
��/mol | 1.0 | 1.5 | 1.0 | 1.0 |
�ټ�������H2O��ƽ��ת����Ϊ_____________���������һλС������
������˵����ȷ����_____________�����ţ�
A��������ѹǿ�㶨����Ӧ�ﵽƽ��״̬
B���������������ܶȺ㶨����Ӧ�ﵽƽ��״̬
C����������H2O��ƽ��ת���ʴ�����������H2O��ƽ��ת����
D������Fe3O4�������H2O��ת����
��4��������3����װ�ø�Ϊ���ݾ��ȣ�������罻��������װ�ã����±�������ʼ���ʣ���ʼʱ��ƽ���ĸ����ʵ���������
Fe | H2O��g�� | Fe3O4 | H2 | |
��ʼ/mol | 3.0 | 4.0 | 0 | 0 |
ƽ��/mol | m | n | p | q |
���ڴ�ƽ����װ���м�������A��B��C����״���µĸ����ʣ�������
Fe | H2O��g�� | Fe3O4 | H2 | |
A/mol | 3.0 | 4.0 | 0 | 0 |
B/mol | 0 | 0 | 1 | 4 |
C/mol | m | n | p | q |
���������淴Ӧ��һ�δﵽƽ��״̬��������װ����H2�İٷֺ������ɴ�С��˳�����еĹ�ϵ��___________����A��B��C��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������������ѧ�߶���ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��ʾ�����缫һΪ̼����һΪ��Ƭ������������ָ�뷢��ƫת����a�����д����������ɣ�������������ȷ����
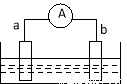
A��aΪ����������Ƭ���ձ��е���ҺΪ����
B��bΪ����������Ƭ���ձ��е���ҺΪ����ͭ��Һ
C��aΪ��������̼�����ձ��е���ҺΪ����
D��bΪ��������̼�����ձ��е���ҺΪ����ͭ��Һ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com