
【题目】下列根据实验操作和现象所得出的结论正确的是

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】向含Al2(SO4)3和AlCl3的混合溶液中逐滴加人1mol/L Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是( )
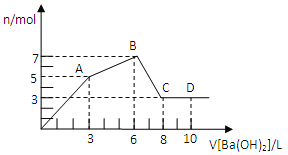
A. 图中C点铝元素存在形式是AlO2—
B. 向D点溶液中通人C02气体,立即产生白色沉淀
C. 原混合液中c[Al2(SO4)3]:c(AlCl3)=1:2
D. OA段反应的离子方程式为:3Ba2++2Al3++8OH-+3SO4=BaSO4↓+2AlO2-+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,下列描述不正确的是( )
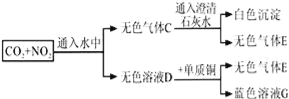
A. C的成分是气体E与二氧化碳的混和气体
B. 浓热的D溶液能把碳单质氧化为二氧化碳
C. 气体E遇空气会被氧化成红棕色的气体
D. 溶液G是蓝色的硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组进行了如图所示的实验,设第一步HNO3的还原产物只有NO.相关分析不正确的是( )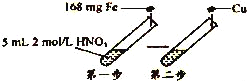
A.第一步反应后溶液中c(NO3﹣)=1.5mol/L(忽略体积变化)
B.第一步反应后溶液中c(Fe2+):c(Fe3+)=1:1
C.第一步可生成标准状况下的气体44.8 mL
D.第二步可溶解铜48mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂、蛋白质为动物性和植物性食物中的基本营养物质。下列说法正确的是
A.蛋白质中只含C、H、O三种元素
B.油脂在人体中发生水解的产物是氨基酸
C.牛油、大豆油的主要成分都是高级脂肪酸甘油脂
D.糖类、油脂、蛋白质一定都能发生水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 电解熔融氯化钠可制金属钠
B. 钠与氧气反应的产物与反应条件无关
C. ClO2可用于自来水的消毒
D. “氯碱工业”是指电解食盐水制取氯气等产品的工业
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下表中各项的排布规律,按此规律排布第23项应为
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
C2H6 | C2H4 | C2H4O2 | C3H8 | C3H6 | C3H6O2 | C4H10 | C4H8 | C4H8O2 | C5H12 |
A.C8H18 B.C9H118O2 C.C9H18 D.C8H16O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.汽油与水不相溶,可以用裂化汽油萃取溴水中的溴
B.石油含有烷烃、环烷烃、芳香烃,煤含有苯、甲苯、二甲苯等有机物
C.煤的气化、液化是使煤变成清洁能源,减小环境污染的有效途径
D.沸点范围:汽油>煤油>柴油>重油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少 8%,氮氧化物(NOx)排放量减少 10%。目前,消除大气污染有多种方法。
(1)用 CH4 催化还原氮氧化物可以消除氮氧化物的污染。
已知:①CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g)△H =-574 kJ/mol
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g)△H =-1160 kJ/mol
③H2O(g) = H2O(l) △H =-44.0 kJ/mol
写出 CH4(g)与 NO2(g)反应生成 N2(g)、CO2(g)和 H2O(l)的热化学方程式:__________。
(2)利用 Fe2+、Fe3+的催化作用,常温下可将 SO2 转化为 SO42-,从而实现对 SO2 的治理。已知含 SO2 的废气通入含 Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为 4Fe2+ + O2 + 4H+ = 4Fe3+ + 2H2O,则另一反应的 离子方程式为__________。
(3)用活性炭还原法处理氮氧化物。有关反应为 C(s) + 2NO(g) ![]() N2(g) + CO2(g)。某研究小组向密闭的真空 容器中(假设容器体积不变,固体试样体积忽略不计)加入 NO 和足量的活性炭,在恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g) + CO2(g)。某研究小组向密闭的真空 容器中(假设容器体积不变,固体试样体积忽略不计)加入 NO 和足量的活性炭,在恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度(mol/L) | NO | N2 | CO2 |
0 | 1.00 | 0 | 0 |
10 | 0.58 | 0.21 | 0.21 |
20 | 0.40 | 0.30 | 0.30 |
30 | 0.40 | 0.30 | 0.30 |
40 | 0.32 | 0.34 | 0.17 |
50 | 0.32 | 0.34 | 0.17 |
①10~20 min 以υ(N2)表示的反应速率为__________。
②该反应的平衡常数表达式 K=________。根据表中数据,计算 T1 ℃时该反应的平衡常数为__________(保留两位小数)。
③一定温度下,随着 NO 的起始浓度增大,则 NO 的平衡转化率__________ (
④下列各项能作为判断该反应达到平衡的是__________ (填序号)。
A.混合气体的密度保持不变
B.υ正(NO) = 2υ逆(CO2)
C.容器内压强保持不变
D.容器内 N2 的体积分数保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com