
【题目】我国科研人员以Zn和尖晶石型锰酸锌( ZnMn2O4)为电极材料,研制出一种水系锌离子电池,该电池的总反应式为xZn+Zn1-xMn2O4![]() ZnMn2O4(0<x<1)。下列说法正确的是( )
ZnMn2O4(0<x<1)。下列说法正确的是( )
A.放电时,Zn2+向负极迁移
B.充、放电过程中,仅锌元素的价态发生变化
C.充电时,阳极的电极反应式为ZnMn2O4 -2xe-=Zn1-XMn2O4+xZn2+
D.若维持电流强度为0.5A,放电10分钟,理论上消耗Zn的质量约为0.20 g (已知F =96500 C/mol)
【答案】C
【解析】
根据电池的电池反应式为:xZn+Zn1-xMn2O4![]() ZnMn2O4(0<x<1),可知,放电时,Zn的化合价升高,被氧化,为原电池的负极,负极的电极反应式:Zn-2e-=Zn2+;正极反应为:Zn1-xMn2O4+xZn2++2xe-═ZnMn2O4,充电时阴阳极反应与负极、正极反应刚好相反,充电时,电解池阳离子向阴极移动,据此分析解答。
ZnMn2O4(0<x<1),可知,放电时,Zn的化合价升高,被氧化,为原电池的负极,负极的电极反应式:Zn-2e-=Zn2+;正极反应为:Zn1-xMn2O4+xZn2++2xe-═ZnMn2O4,充电时阴阳极反应与负极、正极反应刚好相反,充电时,电解池阳离子向阴极移动,据此分析解答。
A.放电时,Zn2+向负电荷较多的正极迁移,A错误;
B.充放电过程中锰元素的化合价也变化,所以充放电过程中锌与锰的化合价变化,B错误;
C.充电时阳极发生氧化反应,与正极反应刚好相反,所以阳极的电极反应为:ZnMn2O4 -2xe-=Zn1-XMn2O4+xZn2+,C正确;
D.若维持电流强度为0.5A,放电10分钟,转移电量Q=0.5×10×60C=300C,假设反应消耗Zn质量为x,则![]() =300,解得x=0.1g,D错误;
=300,解得x=0.1g,D错误;
故合理选项是C。


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案科目:高中化学 来源: 题型:
【题目】纳米磷化钻常用于制作特种钻玻璃,制备磷化钻的常用流程如图:
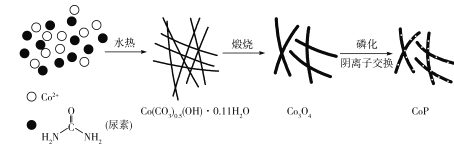
(1)基态P原子的电子排布式为___。P在元素周期表中位于___区。
(2)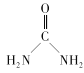 中碳原子的杂化类型是___C、N、O三种元素的第一电离能由大到小的顺序是___(用元素符号表示),电负性由大到小的顺序为___。
中碳原子的杂化类型是___C、N、O三种元素的第一电离能由大到小的顺序是___(用元素符号表示),电负性由大到小的顺序为___。
(3)CO32-中C的价层电子对数为___,其空间构型为___。
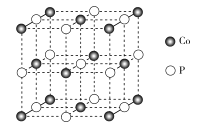
(4)磷化钴的晶胞结构如图所示,最近且相邻两个钴原子的距离为n pm。设NA为阿伏加德罗常数的值, 则其晶胞密度为___g.cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图曲线表示其他条件一定时,反应2NO+O2![]() 2NO2(正反应为放热反应)达平衡时NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是()
2NO2(正反应为放热反应)达平衡时NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是()
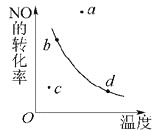
A.a点B.b点C.c点D.d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于热化学方程式:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,下列有关叙述不正确的是( )
A.上述热化学方程式可表示为H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
B.1 mol H2完全燃烧生成液态水时放出285.8 kJ的热
C.2个氢分子完全燃烧生成液态水时放出571.6 kJ的热
D.2 mol H2完全燃烧生成液态水放出571.6 kJ的热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定的温度下,在固定容积的密闭容器中,不能表示反应X(气)+2Y(气)![]() 2Z(气)一定达到化学平衡状态的是( )
2Z(气)一定达到化学平衡状态的是( )
A. 容器内压强不随时间改变B. 容器内混合气体的密度不随时间改变
C. 生成Z的速率与生成Y的速率相等D. 混合气体的平均相对分子质量不随时间改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 1molCO和 2molH2充入一容积为 1L的密闭容器中,分别在250°C、T°C下发生反应:CO(g)+2H2(g) ![]() CH3OH(g)。根据图,下列分析中正确的是( )
CH3OH(g)。根据图,下列分析中正确的是( )
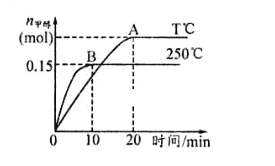
A.平衡时CO的转化率:250°C>T°C
B.该反应的正反应是放热反应
C.反应达平衡后,其他条件不变,若减小容积体积,CO 体积分数增大
D.250°C时,反应在前10s的平均速率υ(H2)=0.015mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向100mL饱和的H2S溶液中通入SO2气体(气体体积换算成标准状况),发生反应:2H2S+SO2=3S↓+2H2O,测得溶液pH与通入SO2的关系如图所示。下列有关说法错误的是( )
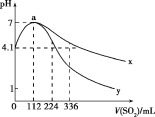
A.a点水的电离程度最大
B.该温度下H2S的Ka1≈10-7.2
C.曲线y代表继续通入SO2气体后溶液pH的变化
D.a点之后,随SO2气体的通入,![]() 的值始终减小
的值始终减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】150℃时,将1L混合烃与9L氧气混合,在密闭容器内充分燃烧,当恢复至150℃时,体积恒定时,容器内压强增大8%,则该混合烃的组成是( )
A.甲烷与乙烷体积比1:4B.甲烷与乙炔体积比1:4
C.乙烯与丁烯体积比1:4D.乙烯与丁烷体积比1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物向![]()
![]() 溶液中滴加
溶液中滴加![]()
![]() 溶液,发现溶液变绿,继续滴加产生棕黄色沉淀,经检验,棕黄色沉淀中不含
溶液,发现溶液变绿,继续滴加产生棕黄色沉淀,经检验,棕黄色沉淀中不含![]() ,含有
,含有![]() 、
、![]() 和
和![]() 。已知:Cu+
。已知:Cu+![]() Cu+Cu2+, Cu2+
Cu+Cu2+, Cu2+![]() CuI↓(白色)+I2。
CuI↓(白色)+I2。
(1)用稀硫酸证实沉淀中含有![]() 的实验现象是___________。
的实验现象是___________。
(2)向洗净的棕黄色沉淀中加入足量KI溶液,产生白色沉淀,继续向上层清液中加入淀粉溶液并没有变蓝的现象出现,请结合离子反应方程式解释不变蓝的原因________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com