
下列离子方程式书写正确的是( )
|
| A. | 向氧化镁中加入硫酸溶液 Mg2++SO42﹣═MgSO4 |
|
| B. | 向水中加入钠块 2Na+2H2O═2Na++2OH﹣+H2↑ |
|
| C. | 向氢氧化钡溶液中加入过量硫酸氢钠溶液 H++SO42﹣+Ba2++OH﹣═BaSO4↓+H2O |
|
| D. | 铁跟稀硫酸反应 2Fe+6H+═2Fe3++3H2↑ |
考点:
离子方程式的书写.
分析:
A.氧化镁为 氧化物,离子方程式中氧化镁不能拆开,硫酸镁为易溶物,离子方程式中不能保留化学式;
B.钠化学性质活泼,与水反应生成氢氧化钠和氢气;
C.硫酸氢钠过量,离子方程式按照氢氧化钡的组成书写;
D.铁与稀硫酸反应生成硫酸亚铁,不是生成铁离子.
解答:
解:A.向氧化镁中加入硫酸溶液,反应生成可溶性的硫酸镁和水,正确的离子方程式为:MgO+2H+═Mg2++H2O,故A错误;
B.钠与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O═2Na++2OH﹣+H2↑,故B正确;
C.氢氧化钡溶液中加入过量硫酸氢钠溶液,离子方程式按照氢氧化钡的组成书写,正确的离子方程式为:2H++SO42﹣+Ba2++2OH﹣═BaSO4↓+2H2O,故C错误;
D.铁与稀硫酸反应生成硫酸亚铁,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故D错误;
故选B.
点评:
本题考查了离子方程式的判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).


科目:高中化学 来源: 题型:
为除去混在氯化钾中的少量硫酸钾和氯化钙杂质,需进行下列六项操作:
①加水溶解②加热蒸发结晶 ③加入过量氯化钡溶液 ④加入过量盐酸 ⑤加入过量碳酸钾溶液 ⑥过滤.
正确的操作顺序是()
A. ①③⑤⑥④② B. ①⑤③④⑥② C. ①③④⑥⑤② D. ①⑤③⑥④②
查看答案和解析>>
科目:高中化学 来源: 题型:
下列能用勒夏特列原理解释的是( )
A.高温及加入催化剂都能使合成氨的反应速率加快
B.红棕色的NO2加压后颜色先变深后变浅
C.SO2催化氧化成SO3的反应,往往需要使用催化剂
D.H2、I2、HI平衡时的混合气体加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验描述,符合事实的是( )
|
| A. | 金属钠暴露在空气中,表面变暗,生成淡黄色固体氧化钠 |
|
| B. | 用坩埚钳夹住打磨过的镁带,在酒精灯上点燃,发出耀眼白光,放出大量的热,产生白色固体 |
|
| C. | 用坩埚钳夹住铝箔在酒精灯上点燃,发出耀眼的白光,放出大量的热 |
|
| D. | 用坩埚钳夹住铝箔在酒精灯上加热至熔化,轻轻晃动,有液态的铝滴落下来 |
查看答案和解析>>
科目:高中化学 来源: 题型:
选择下列实验方法分离物质,将分离方法的序号填在横线上.
A.萃取分液法 B.加热分解法 C.结晶法D.分液法 E.蒸馏法 F.过滤法
(1)分离饱和食盐水与沙子的混合物 .
(2)从硝酸钾和氯化钠的混合溶液中获得硝酸钾 .
(3)分离水和汽油的混合物 .
(4)分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物 .
(5)从碘的水溶液里提取碘 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应的ΔH=+100 kJ·mol-1,下列有关该反应的叙述正确的是( )
A.正反应活化能小于100 kJ·mol-1
B.逆反应活化能一定小于100 kJ·mol-1
C.正反应活化能不大于100 kJ·mol-1
D.正反应活化能比逆反应活化能大100 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
反应N2(g)+3H2(g) 2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线关系如下图,则氨的百分含量最高的一段时间是( )
2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线关系如下图,则氨的百分含量最高的一段时间是( )
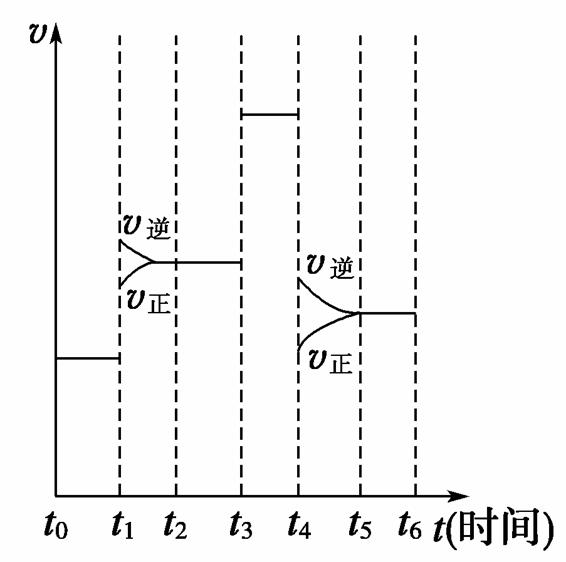
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
查看答案和解析>>
科目:高中化学 来源: 题型:
100mL某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32﹣、SO42﹣、NO3﹣中的几种.①若加入锌粒,会产生H2;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则(1)溶液中一定含有的阳离子有 H ,一定不含有的离子有 .
(2)C→D的离子方程式为 .
(3)由A→B及C→D段有关数据可计算出的某两种离子的物质的量浓度分别为 mol•L﹣1和 mol•L﹣1.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com