
已知金属镁能在CO2中燃烧,反应为2Mg+CO2![]() 2MgO+C,某兴趣小组同学据此反应原理,推测钠也能在CO2中燃烧.为了确定其生成产物并进行实验论证,请你参与以下研究过程.
2MgO+C,某兴趣小组同学据此反应原理,推测钠也能在CO2中燃烧.为了确定其生成产物并进行实验论证,请你参与以下研究过程.
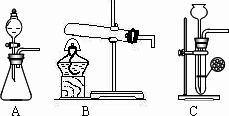
(1)甲同学首先设计了实验室制取二氧化碳的三种发生装置,若选用碳酸氢钠分解制二氧化碳应选用的装置是________(选填装置序号A、B、C,下同);若用石灰石与稀盐酸为原料,并能控制反应随时发生随时停止,最好应选用的装置是________;若用碳酸钠固体与稀硫酸反应应选用的装置是________.
(2)乙同学按实验要求,用下列装置进行实验(已知PdCl2溶液能被CO还原得到黑色的Pd),请回答下列问题:
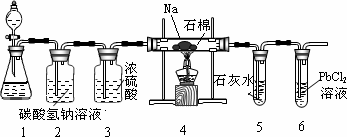
①若装置6中有黑色沉淀,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为___________________.
②若装置6中溶液无明显现象,装置4中残留固体加盐酸后有能使澄清石灰水变浑浊的气体放出(氧元素只在一种生成物中),则钠与二氧化碳反应的化学方程式为_____________.
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
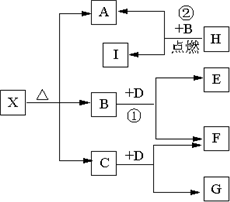 Ⅰ有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的
Ⅰ有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的| 3 | 4 |
 2MgO+C
2MgO+C 2MgO+C
2MgO+C查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
两个研究性学习小组分别根据不同的微型课题进行研究,其方案如下:

Ⅰ.第一个研究性学习小组用如图所示的装置进行镁与二氧化硫反应的实验。
(1)实验室制取二氧化硫类似于制取二氧化碳,在下列物质中选择合适的试剂制取二氧化硫:______________________。
A.10%的硫酸 B.80%的硫酸
C.浓盐酸 D.稀硝酸
E.亚硫酸钠固体 F.亚硫酸钙固体
G.饱和亚硫酸钠溶液
(2)反应后,发现B管壁有淡黄色固体粉末产生,取反应后B中固体溶于稀盐酸中产生具有臭鸡蛋气味的气体,写出B管中发生的有关化学反应方程式:______________________。
(3)你认为该装置是否有不足之处?______________。如果有,请写出改进方法:______________________________。
Ⅱ.第二个研究性学习小组进行了“实验室制硅”的研究,它们以课本为基础,查阅资料得到以下可供参考的信息:①工业上在高温时用木炭粉还原二氧化硅可制得硅 ②镁在点燃条件下即可与二氧化硅反应 ③金属硅化物与稀硫酸反应生成硫酸盐与硅烷 ④硅和二氧化硅均不与稀硫酸反应 ⑤硅烷在空气中能自燃
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥,最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(4)该小组“实验室制硅”的化学方程式是_________________________________________。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;镁和钠的化学性质也有一定的相似性。
两个研究性学习小组分别根据不同的微型课题进行研究,其方案如下:

Ⅰ.第一个研究性学习小组用如图所示的装置进行镁与二氧化硫反应的实验。
(1)实验室制取二氧化硫类似于制取二氧化碳,在下列物质中选择合适的试剂制取二氧化硫:______________________。
A.10%的硫酸 B.80%的硫酸
C.浓盐酸 D.稀硝酸
E.亚硫酸钠固体 F.亚硫酸钙固体
G.饱和亚硫酸钠溶液
(2)反应后,发现B管壁有淡黄色固体粉末产生,取反应后B中固体溶于稀盐酸中产生具有臭鸡蛋气味的气体,写出B管中发生的有关化学反应方程式:______________________。
(3)你认为该装置是否有不足之处?______________。如果有,请写出改进方法:______________________________。
Ⅱ.第二个研究性学习小组进行了“实验室制硅”的研究,它们以课本为基础,查阅资料得到以下可供参考的信息:①工业上在高温时用木炭粉还原二氧化硅可制得硅 ②镁在点燃条件下即可与二氧化硅反应 ③金属硅化物与稀硫酸反应生成硫酸盐与硅烷 ④硅和二氧化硅均不与稀硫酸反应 ⑤硅烷在空气中能自燃
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥,最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(4)该小组“实验室制硅”的化学方程式是_________________________________________。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com