
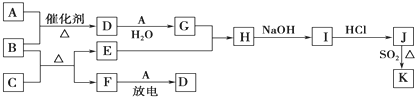
| ||
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
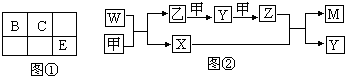
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | HCl的酸性比H2CO3强 | 氯的非金属性大于碳 |
| B | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
| C | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
| D | SiO2可与HF反应 | 氢氟酸不能保存在玻璃瓶中 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 结论 |
| A | 取久置的Na2O2粉末,向其中滴加过量的稀硫酸 | 产生无色气体 | Na2O2没有变质 |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3.H2O能大量共存 |
| C | 将KI和FeCl3溶液在试管中混合后,加入CCl4震荡,静置 | 下层溶液显紫红色 | 氧化性:Fe2+>I2 |
| D | 向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有CO32-或HCO3- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向25mL沸水中滴加5-6滴稀的FeCl3溶液制备氢氧化铁胶体 |
| B、只用少量水就可鉴别Na2CO3和NaHCO3固体 |
| C、用FeSO4、NaOH和盐酸等试剂在空气中可以制备纯净的FeCl3溶液 |
| D、用NaOH溶液和盐酸可除去MgCl2溶液中混有的AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯和溴水振荡后,由于发生化学反应而使溴水的水层颜色变浅 |
| B、酸性高锰酸钾溶液和溴水都既能鉴别出甲烷和乙烯又能除去甲烷中含有的乙烯再经干燥而获得纯净的甲烷 |
| C、煤中含有苯和甲苯,可以用先干馏,后蒸馏的方法把它们分离出来 |
| D、裂化的目的是得到轻质油,裂解的目的是得到乙烯、丙烯等化工原料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com