



 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
| A、X、Y形成的气态氢化物的沸点前者高 |
| B、W、M形成的化合物可作为水处理中的消毒剂 |
| C、工业上通常用电解法制备Z、W、M的单质 |
| D、X、Z形成的化合物ZX3和Z3X所含键的类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
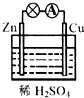 在如图所示的原电池中,正极发生的反应是( )
在如图所示的原电池中,正极发生的反应是( )| A、2H++2e-═H2↑ |
| B、Cu-2e-═Cu2+ |
| C、Cu2++2e-═Cu |
| D、Zn-2e-═Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在强碱存在的条件下,酯在水中的溶解度增大 |
| B、加催化剂,使氮气和氢气在一定条件下转化为氨气 |
| C、可用浓氨水和氢氧化钠固体快速制取氨气 |
| D、500℃左右比室温更有利于合成氨反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com