
| A. | Mg2+、K+、SO42-、OH- | B. | Ba2+、K+、Cl-、CO32- | ||
| C. | Cu2+、Ba2+、Cl-、NO3- | D. | Fe2+、H+、SO42-、MnO4- |
分析 A.镁离子与氢氧根离子反应生成氢氧化镁沉淀;
B.钡离子与碳酸根离子反应生成碳酸钡沉淀;
C.四种离子之间不反应,能够共存;
D.酸性高锰酸根离子能够氧化亚铁离子.
解答 解:A.Mg2+、OH-之间反应生成氢氧化镁沉淀,在溶液中不能大量共存,故A错误;
B.Ba2+、CO32-之间反应生成碳酸钡,在溶液中不能大量共存,故B错误;
C.Cu2+、Ba2+、Cl-、NO3-之间不发生反应,在溶液中能够大量共存,故C正确;
D.MnO4-在酸性条件下具有强氧化性,能够氧化Fe2+,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等,试题培养了学生的灵活应用能力.


 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:选择题
| A. | HCl | B. | BaCl2 | C. | NaOH | D. | Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红的溶液中:CO32-、Na+、AlO2-NO3- | |
| B. | 无色溶液中:K+、Na+、MnO4-、SO42- | |
| C. | 加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+ | |
| D. | 使石蕊变蓝的溶液中:Fe2+、Al3+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaOH的碱性比LiOH的弱 | |
| B. | HCl、HBr、HI的热稳定性依次增强 | |
| C. | HClO4的酸性比H2SO4强说明氯元素的非金属性比硫元素强 | |
| D. | 若M+和R2-的核外电子层结构相同,则原子序数:M>R |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
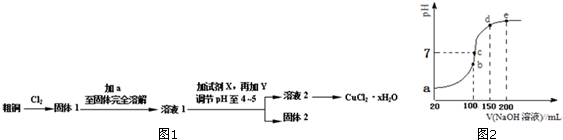
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com