
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
分析 不加其他试剂进行鉴别,则首先需要考虑物质的水溶液的颜色,然后物质间相互滴加的顺序不同,产生不同现象进行鉴别,以此解答.
解答 解:①NaOH滴加到Al2(SO4)3溶液中,先有沉淀后沉淀消失,Al2(SO4)3溶液滴加到NaOH溶液中,先无沉淀后生成沉淀,现象不同,可鉴别,故①正确;
②Na2CO3 和稀HCl滴加顺序不同,现象不同:将Na2CO3 滴加到稀HCl中马上有气体产生,但将稀HCl滴加到Na2CO3 溶液中,先没有气体生成,当滴加到一定程度时,才有气体生成,可鉴别,故②正确;
③Ba(OH)2和H2SO4混合生成硫酸钡沉淀,不能鉴别,故③错误;
④NaAlO2和稀盐酸,当盐酸少量时,离子反应方程式为H++AlO2-+H2O=Al(OH)3↓,当盐酸过量时,离子反应方程式为:4H++AlO2-=Al3++2H2O,所以反应现象不同,故④正确,
故选C.
点评 本题考查了常见物质的鉴别,把握物质的颜色及相互滴加时发生的化学反应为解答的关键,注意物质的性质差异来鉴别物质,题目难度不大.


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:填空题
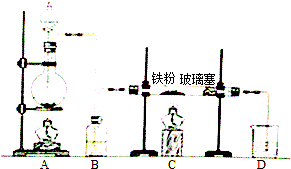 计算:
计算:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、K+、SO42-、OH- | B. | Ba2+、K+、Cl-、CO32- | ||
| C. | Cu2+、Ba2+、Cl-、NO3- | D. | Fe2+、H+、SO42-、MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
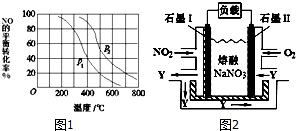
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ”取该试剂瓶中的试剂,通过燃烧实验测得:16.6g 该物质完全燃烧得到39.6g CO2与9g H2O.
”取该试剂瓶中的试剂,通过燃烧实验测得:16.6g 该物质完全燃烧得到39.6g CO2与9g H2O.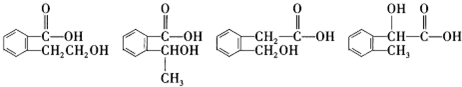 (任写两种).
(任写两种).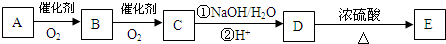
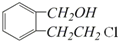 .
.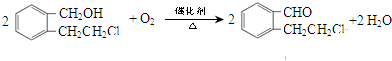 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 淀粉、油脂、蛋白质等天然高分子化合物都可以水解 | |
| B. | 某容器内的物质经科学测定只含有一种元素,则可以断定该物质是一种纯净物 | |
| C. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| D. | 质子数为53,中子数为78的点原子可以表达为:${\;}_{53}^{78}$I |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL 1mol/L FeCl3溶液 | B. | 50mL 0.3mol/L NaCl溶液 | ||
| C. | 10mL 0.2mol/L CaCl2溶液 | D. | 200mL 0.1mol/L NH4Cl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com