
【题目】下列变化必须加入氧化剂才能发生的是
A. Cu2+→Cu B. Cl-→Cl2 C. H2SO4→SO2 D. CO2→CO32-
科目:高中化学 来源: 题型:
【题目】钒是一种熔点很高的金属,具有良好的可塑性和低温抗腐蚀性,有延展性、硬度大,无磁性。广泛应用于钢铁、航空航天、能源、化工等领域。中铝集团 (平果铝业公司)目前使用一种新型工艺,以便从铝业生成的固体废料——赤泥中提取金属钒,具体工艺流程图如下:
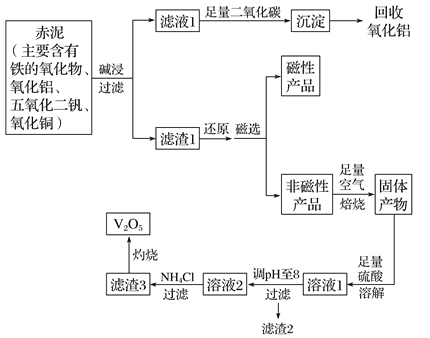
已知:
I.钒有多种价态,其中+5价最稳定。钒在溶液中主要以VO2+和VO3-的形式存在,存在平衡
VO2++H2O![]() VO3-+2H+。
VO3-+2H+。
Ⅱ.部分含钒物质在水中的溶解性如下表所示:
物质 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 难溶 | 难溶 | 易溶 |
Ⅲ.部分离子的沉淀pH值:
Cu2+ | Fe2+ | Fe3+ | |
开始沉淀pH值 | 5.2 | 7.6 | 2.7 |
完全沉淀pH值 | 6.4 | 9.6 | 3.7 |
请回答下列问题:
(1)碱浸步骤中最好选用 。
A.NaOH溶液 B.氨水 C.纯碱溶液
(2)写出滤液1与足量二氧化碳反应的离子方程式 。
(3)磁选步骤得到的磁性产品为 。
(4)溶液1到溶液2的过程中,调节pH值至8有两个目的,一是除去铜离子,二是使 。
(5)滤渣3的主要成分为 ,工业上常用铝热反应法由V2O5冶炼金属钒,请写出反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的A、B两种酸溶液各1 mL,分别加水稀释到1 000 mL,其pH与溶液体积V的关系如图所示。

下列说法正确的是( )
A. A、B两酸溶液的物质的量浓度一定相等
B. 稀释后,A酸溶液的酸性比B酸溶液强
C. a=5时,A是强酸,B是弱酸
D. 若A、B都是弱酸,则5≥a>2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. IA族元素的金属性比IIA族元素的金属性强
B. 第三周期元素的离子半径从左到右逐渐减小
C. 同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D. ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以I—的形式存在。实验室里从海带中提取碘的流程如下:(已知C12+2KI=2KCl+I2)

(1)步骤①的操作方法是________;除漏斗、烧杯外,还需要使用的玻璃仪器是__________。
(2)提取碘的过程中,可供选择的萃取剂是(______)
A、苯、酒精 B、CCl4、苯 C、汽油、醋酸
(3)步骤③的操作中,所用的主要玻璃仪器是_________________。当将含碘有机溶液静置分层后,若要取出下层液体的接下来的操作是:________________________________________
(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏过程,蒸馏实验中用到的主要玻璃仪器有:温度计、牛角管、酒精灯、____________、__________、锥形瓶。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2011年11月,“神舟八号”在酒泉发射升空,并取得圆满成功。“神舟八号”的运载火箭所用燃料是偏二甲肼(C2H8N2)(其中N的化合价为-3)和四氧化二氮(N2O4)。在火箭升空过程中,燃料发生反应:![]() 提供能量。下列有关叙述正确的是
提供能量。下列有关叙述正确的是
A. 该燃料绿色环保,在燃烧过程中不会造成任何环境污染
B. 该反应中N2O4是氧化剂,偏二甲肼是还原剂
C. N2既是氧化产物又是还原产物,CO2既不是氧化产物也不是还原产物
D. 每有0.6 mol N2生成,转移电子数目为2.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的原子最外层有2个电子,该元素( )
A. 一定是金属元素 B. 最高化合价一定为+2价
C. 一定是ⅡA族元素或是He D. 无法确定属于哪类元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲配制两种一定物质的量浓度的NaOH溶液。
(1)用NaOH固体配制l00mL lmol·L-1 NaOH溶液有如下基本操作,C操作的名称是_______________。

(2)该同学用上述lmol·L-1 NaOH溶液配制50 mL 0.lmol·L-1的NaOH溶液。下列仪器中不必要用到的有_______ 。
①托盘天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管
(3)该同学在两次配制中,以下操作使所配溶液的物质的量浓度偏大的是_________:
A.准取称取4.0gNaOH,待溶解后立即转移到100mL容量瓶中并定容
B.定容并摇匀,容量瓶正立后发现液面低于刻度线,继续定容
C.用少量的lmol·L-1 NaOH溶液将50mL容量瓶洗涤2~3次
D.向容量瓶中加水至超过刻度线,用胶头滴管吸出后再定容至l00mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com