
| A.蒸发皿 | B.石棉网 | C.漏斗 | D.烧杯 |
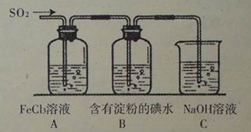
 SO42-+2Fe2++4H+(2分);
SO42-+2Fe2++4H+(2分); CuSO4+2H2O+SO2↑(2分);酸性和氧化性(2分);
CuSO4+2H2O+SO2↑(2分);酸性和氧化性(2分);

 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.得到的沉淀是BaSO4 | B.得到的沉淀是BaSO4和BaSO3 |
| C.一定无BaSO3生成 | D.无沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将SO2通入品红溶液中,溶液褪色 |
| B.将SO2气体通入溴水中,溶液褪色 |
| C.将 SO2气体通入含有氢氧化钠的酚酞溶液中,溶液褪色 |
| D.将SO2气体通入酸性高锰酸钾溶液中,溶液褪色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 SO2外,还可能含有H2和Q气体。为此设计了下
SO2外,还可能含有H2和Q气体。为此设计了下 列探究实验装置(图中夹持仪器省略)。
列探究实验装置(图中夹持仪器省略)。
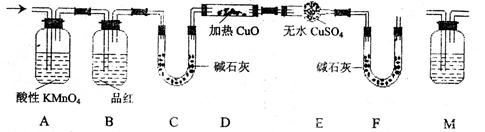

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.S2- | B.S | C.SO32- | D.SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com