
常温下,浓度均为0.1 mol/L的6种盐溶液pH如下:
| 溶质 | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaCl O |
| pH | 11.6 | 9.7 | 12.3 | 10.0 | 4.0 | 10.3 |
下列说法正确的是 ( )
A. Cl2和Na2CO3按物质的量之比1:1反应的化学方程式为:
Cl2+Na2CO3+H2O=HClO+NaHCO3+NaCl
B.相同条件下电离程度比较:HCO3->HSO3->HClO
C.6种溶液中,Na2SiO3溶液中水的电离程度最小
D.NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(HSO3-)>c(SO32‑)>c(OH-)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
“玉兔”号月球车用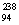 Pu作为热源材料。下列关于
Pu作为热源材料。下列关于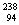 Pu的说法正确的是
Pu的说法正确的是
A.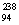 Pu与
Pu与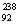 U互为同位素 B.
U互为同位素 B.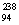 Pu与
Pu与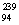 Pu互为同素异形体
Pu互为同素异形体
C.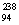 Pu与
Pu与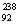 U具有相同的化学性质 D.
U具有相同的化学性质 D.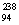 Pu与
Pu与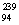 Pu具有相同的最外层电子数
Pu具有相同的最外层电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中,都是强电解质的是 ( )
A.NaOH、Ca(OH)2、NH3·H2O B.NH4Cl、CH3COOH、Na2S
C.HBr、HCl、BaSO4. D.HClO、NaF、Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
在t℃时,某NaOH稀溶液中,c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=13,则在该温度下,将100 mL 0.10 mol/L的稀硫酸与100 mL 0.40 mol/L的NaOH溶液混合后,溶液的pH为(已知:忽略混合时体积的变化;lg2=0.30;lg3=0.48)( )
A.11.52 B.11.70
C.11.82 D.12.00
查看答案和解析>>
科目:高中化学 来源: 题型:
将pH=3的盐酸a L分别与下列三种溶液混合后,混合液均呈中性:
①1×10-3 mol·L-1的氨水b L
②c(OH-)=1×10-3 mol·L-1的氨水c L
③c(OH-)=1×10-3 mol·L-1的Ba(OH)2溶液d L
其中a、b、c、d的关系正确的是 ( )
A.b>a=d>c B.a=b>c>d
C.a=b>d>c D.c>a=d>b
查看答案和解析>>
科目:高中化学 来源: 题型:
有一包粉末可能含有K+、Fe3+、Al3+、Cl-、SO42-、CO32-中的若干种,现进行以下实验:
(1)取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
(2)向(1)溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后在滤液中加入稀硝酸酸化,然后滴入AgNO3溶液,有白色沉淀生成;
(3)取(2)中的有色沉淀加入足量的稀盐酸后,沉淀全部溶解;
(4)重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
(5)向(4)的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤。往得到的沉淀中加入过量的NaOH溶液,沉淀减少。
根据上述实验,这包粉末中一定不含有的离子是 ,肯定含有的离子是 ,不能确定是否含有的离子可通过
(填试验方法)来进一步确定该离子。
步骤(5)中发生反应的离子方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:
葡萄酒常用Na2S2O5作抗氧化剂。中华人民共和国国家标准(G112760-2011)规定葡萄酒中抗氧化剂的残留量(以游离SO2计算)不能超过0.25g/L。某兴趣小组用下图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
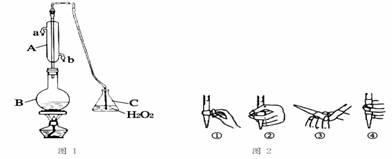
(1)仪器A的名称是 。水通入A的进口为 (填字母)。
(2)B中加人300. 00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应.其化学方程式为 。
(3)除去C中过量的H2O2,然后用0.0900 mol/L NaOH标准溶液进行滴定,滴定前排气泡时,应选择上述图2中的 (填序号);若滴定终点时溶液的pH=8.8,则选择的指示剂为 ;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处时,管内液体的体积 (填序号)(①= 10mL;②=40mL; ③<10mL;④>40mL)
(4)配制100 mL 0. 0900 mol/LNaOH标准溶液的操作如下:
①烧杯中的溶液冷却到室温后,小心转入仪器X中
②将用托盘天平称量好的NaOH固体放入小烧杯中,加适量蒸馏水溶解
③继续加蒸馏水至液面离刻度线1~2 c m处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液都小心转入仪器X中,并轻轻摇匀
⑤将仪器X塞紧,充分摇匀。
上述操作步骤的正确顺序为 (填序号)。仪器X的名称是 。
(5)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为 g/L。
(6)该测定结果比实际值偏高.可能的原因是 ,利用现有装置提出改进的措施为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com