
| A、KMnO4酸性溶液 |
| B、FeCl3溶液 |
| C、溴水 |
| D、金属钠 |


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
| A、等体积、等物质的量浓度的NaHCO3溶液和Ca(OH)2溶液混合:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
| B、向漂白粉中通入少量的SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| C、过量的Fe与稀硝酸反应:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O |
| D、过量的SO2通入到Ba(NO3)2溶液中:3SO2+2NO3-+3Ba2++2H2O═3BaSO4↓+2NO↑+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯、苯都可与溴水发生加成反应 |
| B、乙醇、乙烯都可被酸性高锰酸钾溶液氧化 |
| C、乙醇、乙酸都可以发生酯化反应 |
| D、淀粉、油脂、蛋白质都可以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液中一定存在:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
| B、该溶液中可能存在:c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
| C、向该溶液中滴入少量稀盐酸,一定会产生气泡 |
| D、向该溶液中滴入少量Ca(OH)2溶液,一定会有白色沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新能源汽车的推广与使用有助于减少光化学烟雾的产生 |
| B、酸雨形成的主要原因是汽车尾气的任意排放 |
| C、推广煤的气化、液化技术,提供清洁高效燃料 |
| D、用K2FeO4取代Cl2处理饮用水,有杀菌消毒作用,且不会形成致癌物,但无净水作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
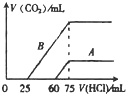
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com