
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高二上期中文化学卷(解析版) 题型:选择题
下列关于金属腐蚀的叙述正确的是
A.金属腐蚀的实质是金属的原子失去电子变成金属离子
B.金属的化学腐蚀必需在酸性条件下进行
C.金属腐蚀的快慢与温度高低无关
D.钢 铁在弱酸性或中性环境腐蚀时,正极上发生的反应是2H++2e-=H2↑
铁在弱酸性或中性环境腐蚀时,正极上发生的反应是2H++2e-=H2↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第二次月考化学试卷(解析版) 题型:填空题
实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反 应:
应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mo
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mo l-1)的变化:
l-1)的变化:
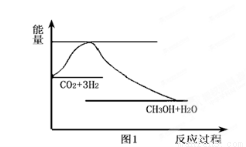
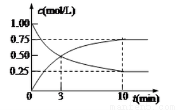
图2
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH
CH3OH (g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如上图2所示。
(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2) = ;
②下列措施中能使化学平衡向正反应方向移动的是 (填字母)。
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.再充入l molCO2和4 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式: 。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极的电极反应式是: 。
。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:选择题
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的①NaOH固体 ②H2O ③NH4Cl固体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
A.①② B.②④⑥ C.②③⑤ D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.质子数为6,中子数为7的原子的元素符号可表示为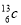
B.H2、SO2、CO三种气体都可用浓硫酸干燥
C.共价化合物溶于水,分子内共价键被破坏,单质溶于水,分子内共价键不被破坏
D.陶瓷、玻璃、水泥、大理石的主要成分都是硅酸盐
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试文化学试卷(解析版) 题型:选择题
光纤通信是一种现代化的通信手段,制造光导纤维的主要原料是( )
A.CaCO3 B.Si C.Na2CO3 D.SiO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东深圳高级中学高一上期中考试化学试卷(解析版) 题型:选择题
下列离子方程式中只能表示一个化学反应的是( )
①Ag++Cl-=AgCl↓ ②Fe+Cu2+=Fe2++Cu ③CaCO3+2H+=CO2↑+H2O+Ca2+
④Ba2++2OH-+2H++SO42—=BaSO4↓+2H2O ⑤Fe2++SO42-+Ba2++2OH-=Fe(OH)2↓+BaSO4↓
A.①③ B.⑤ C.④⑤ D.②
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中文化学试卷(解析版) 题型:?????
不属于高分子化合物的是( )
A.淀粉 B.纤维素 C.蛋白质 D.油脂
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上学期期中考试化学试卷(解析版) 题型:选择题
在一个容积为2L的密闭容器中,加入0.8molA2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+ B2(g)====2AB(g)ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说明不正确的是 ( )
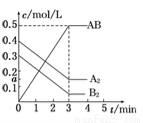
A.图中a点的值为0.15
B.该反应的平衡常数K=0.03
C.温度升高,平衡常数K值减小
D.平衡时A2的转化率为62.5%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com