
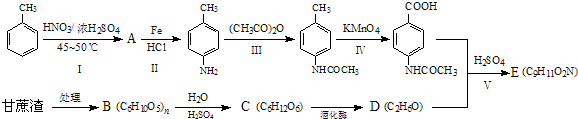
 ),
), 中的硝基被还原成氨基,得
中的硝基被还原成氨基,得 ,
, 与乙酐反应形成酞键,得到
与乙酐反应形成酞键,得到 ,
, 中的甲基被高锰酸钾氧化得
中的甲基被高锰酸钾氧化得 ,
, 中的羧基与乙醇发生酯化同时酞键水解发生取代反应得
中的羧基与乙醇发生酯化同时酞键水解发生取代反应得 ,据此答题;
,据此答题; ),
), 中的硝基被还原成氨基,得
中的硝基被还原成氨基,得 ,
, 与乙酐反应形成酞键,得到
与乙酐反应形成酞键,得到 ,
, 中的甲基被高锰酸钾氧化得
中的甲基被高锰酸钾氧化得 ,
, 中的羧基与乙醇发生酯化同时酞键水解发生取代反应得
中的羧基与乙醇发生酯化同时酞键水解发生取代反应得 ,
, ,
, ;
; ,
, ;
; ,
, ;
;


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案科目:高中化学 来源: 题型:
| A、①>②>③ |
| B、③>②>① |
| C、②>①>③ |
| D、③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所消耗的硝酸的量:①>②>③ |
| B、对环境造成的危害,③最小 |
| C、因铜与浓硝酸作用最快,故制取硝酸铜的最佳方案是① |
| D、三种途径所消耗的铜的质量不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 | ||||
B、用铜作电极电解稀硫酸,反应Cu+H2SO4
| ||||
| C、铅蓄电池放电时的负极和充电时的阳极均发生还原反应 | ||||
| D、使用催化剂,可加快反应速率,改变反应限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将2mol/L NaAlO2溶液和3mol/L的HCl溶液等体积互相均匀混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |
| B、向1mol/L明矾溶液50mL中滴入数滴0.1mol/L Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| C、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
| D、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
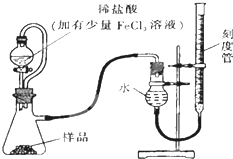 过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.查看答案和解析>>
科目:高中化学 来源: 题型:
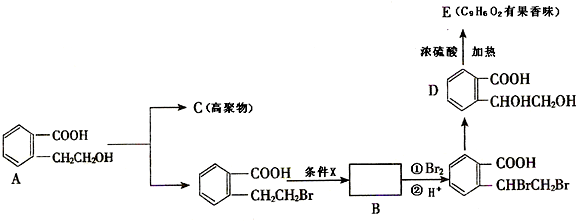
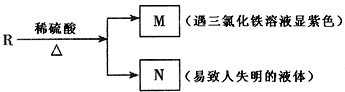
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com