
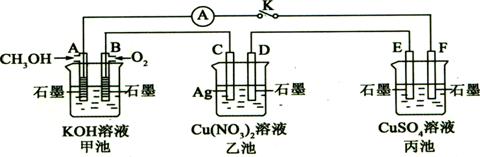
ij��ȤС���ͬѧ����ͼ��ʾװ���о��йص绯ѧ������(�ס��ҡ�����������������)�����պϸ�װ�õĵ��Kʱ���۲쵽�����Ƶ�ָ�뷢����ƫת��
 |
��ش��������⣺
��1���׳�Ϊ (�ԭ��ء��������ء���Ƴء�)��A�缫�ĵ缫��ӦʽΪ ��
��2��������F�缫Ϊ (�����������������������������������)���óص��ܷ�Ӧ��ѧ����ʽΪ ��
��3�����ҳ���C����������10.8 gʱ���׳���B�缫����������O2�����Ϊ mL(��״��)��
��4��һ��ʱ��Ͽ����K������������ʹ�ҳػָ�����ӦǰŨ�ȵ��� (��ѡ����ĸ)��
A��Cu B��CuO C��Cu(OH)2 D��Cu2(OH)2CO3

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��ȷ����
A���⻯����Һ��������ˮ��Ӧ��2I-+ Br2 �� 2Br-+ I2
B��������ˮ�ķ�Ӧ��Cl2+ H2O �� Cl- + ClO- + 2H+
C������ϡ���ᷴӦ��2Fe+ 6H+�� 2Fe3+ + 3H2��
D������������������Һ�ķ�Ӧ��Cl2 + OH-��Cl-+ ClO-+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����Ӧ����һ����ϩ��ֱ���Ʊ������������·�����
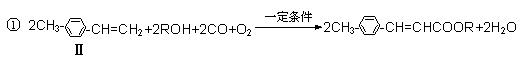 |
������II�ķ���ʽΪ____________��1mol������II����_______mol H2ǡ����ȫ��Ӧ���ɱ���������
��2���ۺ���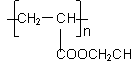
 �������Ʊ�Ϳ�ϣ��䵥��ṹ��ʽΪ_______________��
�������Ʊ�Ϳ�ϣ��䵥��ṹ��ʽΪ_______________��
�������Ʒ�Ӧ�ٵķ�����������ϩΪ�л���ԭ�Ϻϳɸõ��壬�漰�ķ�Ӧ����ʽΪ_______________________________________��_______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
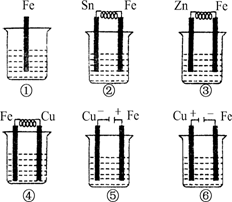
����ͼ��ʾ�����ձ���ʢ�к�ˮ����(������C)�����б���ʴ�ɿ쵽����˳��Ϊ�� ��
A���ڢ٢ۢܢݢ� B���ݢܢۢ٢ڢ�
C���ݢܢڢ٢ۢ� D���ݢۢڢܢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
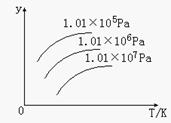
��ͼ��ʾ�¶ȡ�ѹǿ������ƽ���Ӱ�죺N2 (g)��3H2(g)  2NH3(g) ��H��0
2NH3(g) ��H��0
ͼ��y���ʾ�������ǣ� ��
A. ����Ӧ����
B. ƽ����������NH3�ĺ���
C. ƽ����������N2�����ʵ���
D. H2��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪H2O (g) == H2O (l) ��H1����Q1 kJ��mol-1 ��CH3OH(g) == CH3OH(l) ��H2����Q2 kJ��mol-1
2CH3OH(g) +3O2(g) == 2CO2(g)��4H2O(g) ��H3����Q3 kJ��mol-1 ��Q1��Q2��Q3������0����Ҫʹ32gҺ̬�״���ȫȼ�գ����ָ������£��ų�������Ϊ�� ��
A. Q1��Q2��Q3 B. 0.5Q3��Q2��2Q1
C. 0.5Q3��Q2��2Q1 D. 0.5(Q1��Q2��Q3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ͼ��C%��ʾij��Ӧ������ϵ�еİٷֺ�����v��ʾ��Ӧ���ʣ�p��ʾѹǿ��t��ʾ��Ӧʱ�䡣ͼAΪ�¶�һ��ʱѹǿ�뷴Ӧ���ʵĹ�ϵ���ߣ�ͼBΪѹǿһ��ʱ���ڲ�ͬʱ��C%���¶ȵĹ�ϵ���ߡ�ͬʱ������������ͼ��ķ�Ӧ�ǣ� ��
A��N2O3(g) NO2(g)��NO(g) ��H��0
NO2(g)��NO(g) ��H��0
B��4NH3(g)��5O2(g) 4NO(g)��6H2O(g) ��H��0
4NO(g)��6H2O(g) ��H��0
C��3NO2(g)��H2O(l) 2HNO3(aq)��NO(g) ��H��0
2HNO3(aq)��NO(g) ��H��0
D��2CO(g) CO2(g)��C(s) ��H��0
CO2(g)��C(s) ��H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£�ˮ�����ӻ�ΪKW������˵����ȷ����(����)��
A����pH=11����Һ�У�ˮ�������c(OH��)һ������10��3mol/L
B����pH=1������Һ��pH=13�ļ���Һ�������Ϻ����Һ��pHһ������7
C�������ʵ���Ũ�Ⱥ��������ͬ��һԪ��HA��һԪ��BOH��Ϻ���Һ�����ԣ���Ӧ����Һ��c(H��) =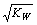
D����ǿ�ᡢǿ���кͺ���Һ��pH=7�����к�ǰ�ᡢ���pH֮��һ������14
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��200mL��������Һ�У�����1.5NA����������ӣ�NA��ʾ����ӵ�����ֵ����ͬʱ����NA���������ӡ���Al2(SO4)3�����ʵ���Ũ��Ϊ�� ��
A��2mol·L-1 B��2.5 mol·L-1 C��5 mol·L-1 D��7.5 mol·L-1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com