
����Ŀ����ͼ��ʵ��������ͭ��Ũ������ȡ��������̽���������ʣ���ش��������⣺
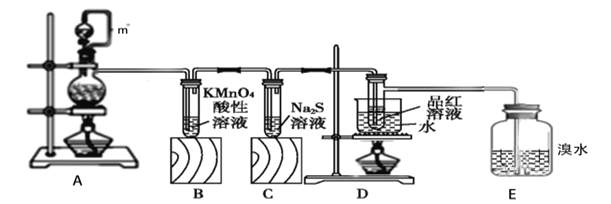
��1��װ��A��m������___��װ��A�������Ե�һ������___��
��2��װ��A�з����Ļ�ѧ��Ӧ����ʽ___���÷�Ӧ������������__________��
��3��װ��B�е�����________��֤��SO2����________��
��4��װ��C����Һ�ڿ����в��ױ��棬ʱ�䳤�˻���ֻ��ǣ�ԭ����_______���������ӷ���ʽ��ʾ��
��5��װ��D��Ŀ����̽��SO2��Ʒ�����õĿ����ԣ�д��ʵ�����������__��
��6��E�е�������___�������Ļ�ѧ��Ӧ����ʽ_______��
���𰸡�ƽ����ѹ��ʹҺ��˳���� ������ƿ�е�Һ�峬�����������������2/3 Cu+2H2SO4(Ũ)![]() CuSO4+2SO2��+2H2O CuSO4 KMnO4 ��Һ��ɫ����ɫ�����ɫ�� ��ԭ�� 2S2-+O2+2H2O��2S��+4OH- Ʒ����Һ��ɫ�رշ�Һ©�����������ٵ�ȼ�ƾ��ƣ���Һ��ɺ�ɫ ��ˮ��ɫ SO2+Br2+2H2O=2HBr+H2SO4
CuSO4+2SO2��+2H2O CuSO4 KMnO4 ��Һ��ɫ����ɫ�����ɫ�� ��ԭ�� 2S2-+O2+2H2O��2S��+4OH- Ʒ����Һ��ɫ�رշ�Һ©�����������ٵ�ȼ�ƾ��ƣ���Һ��ɺ�ɫ ��ˮ��ɫ SO2+Br2+2H2O=2HBr+H2SO4
��������
��1��װ��A��m������Ϊƽ����ѹ��ʹҺ��˳���£�����������ƿʹ�ù���������ƿ����ʢ��Һ�岻�ܳ������ݻ���2/3��Ҳ��������1/3��ͼ���Ѿ��������ݻ���2/3��
��Ϊ��ƽ����ѹ��ʹҺ��˳���£�������ƿ�е�Һ�峬�����������������2/3��
��2��װ��A��ͭ��Ũ������ȡ�����������Ļ�ѧ��Ӧ����ʽΪCu+2H2SO4(Ũ)![]() CuSO4+2SO2��+2H2O���÷�Ӧ��Cu��0�۱�Ϊ+2�ۣ�ʧ���ӣ�������������������CuSO4��
CuSO4+2SO2��+2H2O���÷�Ӧ��Cu��0�۱�Ϊ+2�ۣ�ʧ���ӣ�������������������CuSO4��
��Ϊ��Cu+2H2SO4(Ũ)![]() CuSO4+2SO2��+2H2O��CuSO4��
CuSO4+2SO2��+2H2O��CuSO4��
��3��װ��A������SO2���壬SO2���л�ԭ�ԣ����徭��װ��B�е�����KMnO4 ��Һ����������ԭ��Ӧ��KMnO4 ��Һ��ɫ����ɫ�����ɫ����
��Ϊ��KMnO4 ��Һ��ɫ����ɫ�����ɫ������ԭ�ԣ�
��4��װ��C��ΪNa2S��Һ��S2-���л�ԭ�ԣ������ױ�������O2�������ɵ���S��ʱ�䳤�˻���ֻ��ǣ������ӷ���ʽ��ʾ��2S2-+O2+2H2O��2S��+4OH-��
��Ϊ2S2-+O2+2H2O��2S��+4OH-
��5��װ��D��Ŀ����̽��SO2��Ʒ�����õ�Ư�����ǿ���ģ�ʵ�����������Ϊ��Ʒ����Һ��ɫ�رշ�Һ©�����������ٵ�ȼ�ƾ��Ƽ��ȣ���Һ��ɺ�ɫ��
��6�����ɵ�SO2ͨ�뵽E��SO2����ˮ����������ԭ��Ӧ����ˮ��Һ��ɫ�������Ļ�ѧ��Ӧ����ʽΪSO2+Br2+2H2O=2HBr+H2SO4��
��Ϊ����ˮ��Һ��ɫ��SO2+Br2+2H2O=2HBr+H2SO4



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������0.27kg��������Ϊ10%��CuCl2��Һ���Լ��㣺
��1����Һ��CuCl2�����ʵ���_______��
��2����Һ��Cu2+��Cl-�����ʵ���_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڶ������Ƿǽ���Ԫ���������ڣ��ش��������⡣
(1)����������У�Bԭ����3���ǻ��������侧�������ʯī���ƵIJ�״�ṹ����ͬ����Ӽ����Ҫ��������___________________
(2)��һ�����ܽ���B��N֮��ĵڶ�����Ԫ����_________________�֡�
(3)HNO3�����Ա�HNO2ǿ���Դӽṹ�ĽǶȽ�����ԭ��_____________________
(4)̼���ͬ���壬�����Ľṹͬ���ʯ��ͬ���Ʋ����۵�Ƚ��ʯ��________���ߡ��ͣ������ԭ�ӵİ뾶Ϊr����辧�徧�����ⳤΪ_______________���ô�r����ʽ��ʾ���������Ŀռ�������Ϊ______________��������λ��Ч���֣�
(5)ʯīϩ�����R�����γ�һ�ֲ�㻯�������R��ƽ����ʯī�㣬������ͼ����ʾ���䴹ֱ��ʯī�㷽���ͶӰ��ͼ����ʾ����ò�㻯����Ļ�ѧʽΪ_____��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ������� 6 �������е�ij���֣�Cl-��SO42-��CO32-��NH4+��Na+��K+��Ϊ��ȷ����Һ����ɣ�����������ʵ�飺
��ȡ 200mL ������Һ���������� BaCl2��Һ����Ӧ�������ˡ�ϴ�ӡ�����ó��� 4.30g��������м�����������ᣬ��2.33g�������ܽ⡣
����ٵ���Һ�м�������NaOH��Һ�����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ����������1.12L ���ѻ���ɱ�״�����ٶ�����������ȫ���ݳ�����
��ԭ��Һ��ɫ��Ӧ�ʻ�ɫ��
����ԭ��Һ��ɵĽ��ۣ�����ȷ����
A.һ������Cl-��SO42-��CO32-��NH4+�����ܴ���Na+��K+
B.���ٴ����������ӣ���c(Cl-)��0.05mol/L
C.c(CO32-)=0.05mol/L
D.c(NH4+)��c(SO42-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��t��ʱ����֪PdI2��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ���ǣ� ��
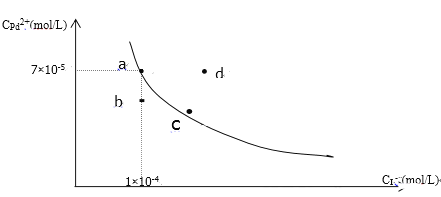
A. ��t��ʱPdI2��Ksp=7.0��10-9
B. ͼ��a���DZ�����Һ��b��d�����Ӧ����Һ���Dz�������Һ
C. ��a�����Һ�м�������NaI���壬��Һ��a����c�㷽���ƶ�
D. Ҫʹd���ƶ���b����Խ����¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����2L�ܱ������У���ʼͶ��4 molN2��6molH2��һ������������NH3��ƽ��ʱ���ı��¶Ȳ�õ����������ʾ����֪��T1<T2��
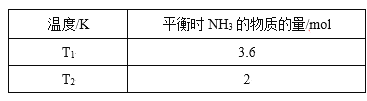
����K1______K2�����>������<����=����ԭ��_______��
����T2�£�����10s�ﵽ��ѧƽ��״̬����0��10s��N2��ƽ������v(N2)Ϊ______��ƽ��ʱH2��ת����Ϊ______������ͬʱ���Ӹ����ʵ���Ϊ1 mol���÷�Ӧ��ƽ��V��_____V����(>��=��<)ƽ�ⳣ����_____�����������С�����䡱��
��������˵���÷�Ӧ�Ѵﵽƽ��״̬����___��
A.3v��H2������2v��NH3���� B.����������ѹǿ����
C.��������ƽ����Է����������ٸı��״̬ D.��H���ֲ���
��2����֪���л�ѧ���ļ���д����ҵ���ư����Ȼ�ѧ����ʽ��
��ѧ�� | H-H | N��N | N-H |
����/kJ��mol-1 | 430 | 936 | 390 |
�Ȼ�ѧ����ʽ��__________��
��3�������ǿ���С����Ƶ�һ����������ԭ��أ����ߵ���Ӱ����Ϊa��b���Ե缫���ֱ��õ������ձ���m��n�����Ե缫�������ӣ�����ԭ��ʾ��ͼ��ͼ��
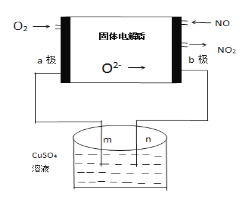
��aΪ___����b���ĵ缫��Ӧʽ____________��
���ڱ�״���£�ͨ��112mL��O2���ɹ۲쵽�ձ���n����_____���ɣ��������ձ��е���Һ�����Ϊ200mL��������䣩���Ӧ��ֹʱ�ձ�����Һ��PHΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ���������ֵ������˵����ȷ����(����)
A.���³�ѹ�£�8 g O2����4NA������
B.1 L 0.1 mol��L��1�İ�ˮ����0.1NA��NH4+
C.��״���£�22.4 L���Ậ��NA��HCl����
D.1 mol Na����ȫ��������Na2O2��ʧȥ2NA������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�����������˵����ȷ����
A. ���³�ѹ�£�8gO2��O3�Ļ�����庬��4NA������
B. 1L0.1mol/L��FeCl3��ȫˮ�⣬�γ�0.1NA��Fe(OH)3��������
C. ��״���£�22.4LCl2ͨ��ˮ�з�����Ӧ��ת�Ƶĵ�����ΪNA
D. 1molNa����ȫ��������Na2O2��ʧȥ��2NA����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ᾧˮ����Ļ�ѧʽΪR��nH2O������Է�������ΪM��25��ʱ��ag�þ����ܹ�����bgˮ���γ�V mL������Һ�����й�ϵ�в���ȷ���ǣ� ��
A.����Һ���ܶ�Ϊ����![]() g��L-1
g��L-1
B.����Һ�����ʵ���Ũ��Ϊc��![]() mol��L-1
mol��L-1
C.����Һ�����ʵ���������Ϊw��![]() %
%
D.25��ʱR���ܽ��S=![]() g
g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com