
【题目】3.2g铜与过量的硝酸(8mol/L,30mL)充分反应,硝酸的还原产物是NO和NO2 , 反应后溶液中含有amolH+ , 则此时溶液中含有NO3﹣的物质的量为( )
A.(0.1+a)mol
B.(0.2+a)mol
C.(0.05+a)mol
D.amol
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】我国正在推广使用乙醇汽油。所谓乙醇汽油就是在汽油中加入适量乙醇(一般为10:l)混合而成的一种燃料。下列有关叙述错误的是
A. 由石油可以制得汽油
B. 乙醇汽油是一种新型的化合物
C. 汽车使用乙醇汽油可以减少有害气体的排放
D. 由玉米、高梁发酵可以制得乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A,B,C,D,E五种短周期元素,已知相邻的A,B,C,D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同.
回答下列问题: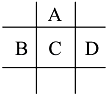
(1)A与E形成的化合物的化学式是 .
(2)B的最高价氧化物化学式为 , C的元素名称为 , D的单质与水反应的方程式为
.
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是 , 有关反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于合金的下列说法不正确的是
A.合金具备金属的特性
B.合金的硬度一般比其组成成分金属的硬度大
C.合金的熔点一般比其组成成分的熔点低
D.合金只能由两种或两种以上的金属组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2-硝基-1,3-苯二酚是橘黄色固体,易溶于水、溶液呈酸性,沸点为88℃,是重要的医药中间体。实验室常以间苯二酚为原料分以下三步合成:

具体实验步骤如下:
①磺化:称取5.5g碾成粉状的间苯二酚放入烧杯中,慢慢加入浓硫酸并不断搅拌,控制温度为60~65℃约15min。
②硝化:将烧杯置于冷水中冷却后加入混酸,控制温度(25±5) ℃左右继续搅拌15min。
③蒸馏:将反应混合物移入圆底烧瓶B中,小心加入适量的水稀释,再加入约0.1g尿素,然后用下图所示装置进行水蒸气蒸馏;将馏出液冷却后再加入乙醇-水混合剂重结晶。
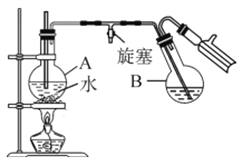
回答下列问题:
(1)实验中设计Ⅰ、Ⅲ两步的目的是__________。
(2)烧瓶A中玻璃管起稳压作用,既能防止装置中压强过大引起事故,又能_______
(3)步骤②的温度应严格控制不超过30℃,原因是_____________。
(4)步骤③所得2-硝基-1,3-苯二酚中仍含少量杂质,可用少量乙醇-水混合剂洗涤。请设计简单的实验证明2-硝基-1,3-苯二酚已经洗涤干净:______________。
(5)本实验最终获得1.0g橘黄色固体,则2-硝基-1,3-苯二酚的产率约为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氢荆芥内酯是有效的驱虫剂。其合成路线如下:
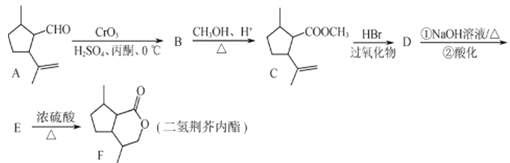
(1)A中有____个手性碳原子,B的结构简式为________。
(2)写出D在NaOH溶液中加热发生反应的化学方程式:____________。
(3)E中含氧官能团的名称是______。
(4)某物质X:①分子组成比A少2个氢原子;②分子中有4种不同化学环境的氢原子;③能与FeCl3溶液发生显色反应。写出所有符合上述条件的物质X的结构简式:__________。
(5)写出由![]() 制备
制备![]() 的合成路线图(无机试剂任选)______。合成路线流程图示例如下:
的合成路线图(无机试剂任选)______。合成路线流程图示例如下:![]()
![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置,能完成很多电化学实验。下列有关此装置的叙述中,不正确的是
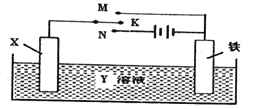
A. 若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B. 若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动
C. 若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D. 若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟电解法处理含六价铬的工业废水,用如图装置将主要有害物Cr2O72-转化为Cr3+(无害)除去。得到如下实验结果:

实验 | 实验条件 | Cr2O72- |
① | A电极为石墨 | 0.922% |
② | A电极为石墨,废水中加入1mL浓硫酸 | 12.7% |
③ | A电极为铁,废水中加入1mL浓硫酸 | 57.3% |
下列说法中,正确的是
A. 对比实验①②可知,升高pH可以提高Cr2O72-的去除率
B. 实验②中, Cr2O72-在阳极放电,电极反应式为Cr2O72-+6e-+14H+=2Cr3++7H2O
C. 对比实验②③可知, Cr2O72-去除率增大的原因是A电极产生的Fe2+也能还原Cr2O72-
D. 实验③中,理论上电路中每通过6mol电子,则有1mol Cr2O72-被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 医用酒精的浓度通常是95%
B. 食用花生油和鸡蛋清都能发生水解反应
C. 淀粉、纤维素和油脂都属于天然高分子化合物
D. 合成纤维和光导纤维都是新型无机非金属材料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com