
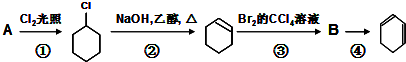
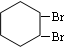
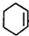
 ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成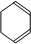 ,据此解答.
,据此解答. ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成 ,据此
,据此 ,故答案为:
,故答案为: ;
; 发生消去反应生成
发生消去反应生成 ,故答案为:消去反应;
,故答案为:消去反应;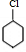 +NaOH
+NaOH| 醇 |
| △ |
 +NaCl+H2O,故答案为:
+NaCl+H2O,故答案为: +NaOH
+NaOH| 醇 |
| △ |
 +NaCl+H2O.
+NaCl+H2O.


科目:高中化学 来源: 题型:
| 物质 编号 | 物质转化关系 | A | D | E |
| ① | 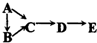 | Si | SiO2 | H2SiO3 |
| ② | N | NO2 | HNO3 | |
| ③ | S | SO2 | H2SO4 | |
| ④ | Na | Na2O2 | NaOH |
| A、①②③④ | B、②③ |
| C、①③④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
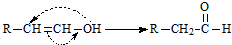 化学式为C9H10O2的有机物A有如下的转化关系
化学式为C9H10O2的有机物A有如下的转化关系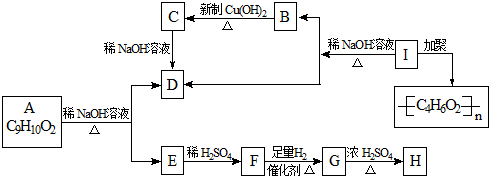
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
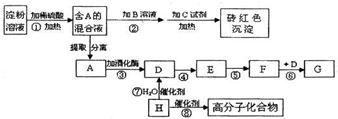
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④⑥ | B、①③⑥⑦ |
| C、②④⑤⑧ | D、②⑤⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
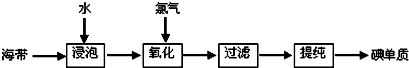
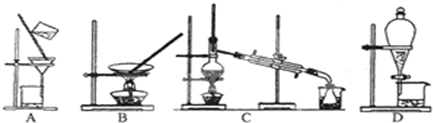
查看答案和解析>>
科目:高中化学 来源: 题型:
A、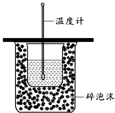 用如图装置测定中和热 |
| B、中和滴定过程中,眼睛应注视锥形瓶内溶液颜色的变化 |
| C、研究H+浓度对该平衡:Cr2O72-+H2O?2CrO42-+2H+的影响,往5mL 0.1mol/L K2CrO4溶液加入5mL 0.1mol/L的稀硫酸 |
| D、测定溶液的pH值时,用玻璃棒蘸取少量溶液点在湿润的pH试纸上再与标准比色卡对照 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com