
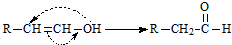 化学式为C9H10O2的有机物A有如下的转化关系
化学式为C9H10O2的有机物A有如下的转化关系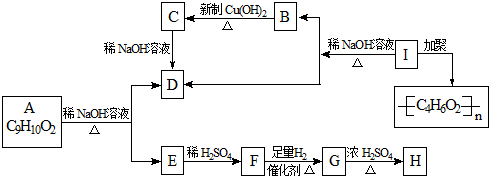
| 2×4+2-6 |
| 2 |
| 2×9+2-10 |
| 2 |
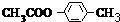 ,故E为
,故E为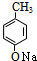 ,F为
,F为 ,G为
,G为 ,H为
,H为 ,据此解答.
,据此解答.| 2×4+2-6 |
| 2 |
| 2×9+2-10 |
| 2 |
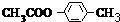 ,故E为
,故E为 ,F为
,F为 ,G为
,G为 ,H为
,H为 ,
, ,H为
,H为 ,I为CH3COOCH=CH2,
,I为CH3COOCH=CH2, ;
; ;CH3COOCH=CH2;
;CH3COOCH=CH2;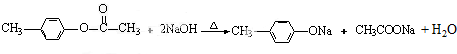 ,
,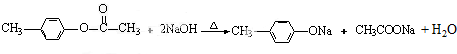 ;
;

 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
| A、常温常压下,11.2L氧气所含的原子数为NA |
| B、1L0.5mol/L的HCl溶液中HCl分子数为0.5NA |
| C、常温常压下,32g氧气所含的氧原子数为2NA |
| D、18g NH4+所含的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
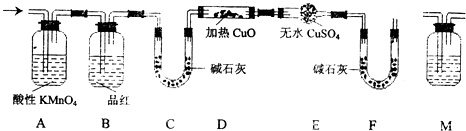
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X与Y形成化合物时,X显负价,Y显正价 |
| B、X的第一电离能大于Y |
| C、X的原子序数小于Y |
| D、气态氢化物的稳定性X强于Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| H2O |
| H+ |
| Cl2 |
| 光照 |
| NaOH |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.00 | 31.00 |
| 2 | 20.00 | 1.00 | 32.04 |
| 3 | 20.00 | 1.10 | 32.18 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com