
【题目】(1)在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:
①混合气体的平均摩尔质量是___________________。
②混合气体中所含碳原子的物质的量是_____________________。
③CO2和CO的体积之比是_______________________。
(2)标准状况下有①0.112 L水 ②0.5NA个HCl分子③25.6 g SO2气体 ④0.2 mol氨气(NH3) ⑤2 mol He 所含原子个数从大到小的顺序为__________________。
(3)将质量分数为a%,物质的量浓度为c1 mol·L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是_______________。(用含c1 和c2的代数式表示)
(4)某温度时,一定量的元素A的气态氢化物AH3,在恒温密闭容器中分解为两种气体单质,此时压强增加了75%,则AH3分解反应的化学方程式________________________。
【答案】(1) 30 g·mol-1 0.5 mol 1∶7
(2)①>⑤>③>②>④ (3)2c1<c2(3分)(3)4AH3=A4+6H2(3分)
【解析】
试题分析:(1)①混合气体的物质的量=11.2L÷22.4L/mol=0.5mol,因此混合气体的平均摩尔质量=15g÷0.5mol=30g/mol。
②根据一氧化碳和二氧化碳的分子式可知混合气体中所含碳原子的物质的量是0.5mol。
③设混合气体中CO2和CO的物质的量分别是xmol、ymol,则x+y=0.5、44x+28y=15,解得x=1/16、y=7/16,所以体积之比是1∶7。
(2)①0.112 L水的物质的量是![]() ,所含原子的物质的量是6.2mol×3=18.6mol;0.5NA个HCl分子中原子的物质的量是1mol;25.6 g SO2气体中原子的物质的量是
,所含原子的物质的量是6.2mol×3=18.6mol;0.5NA个HCl分子中原子的物质的量是1mol;25.6 g SO2气体中原子的物质的量是![]() ;0.2 mol氨气(NH3)分子中含有的原子的物质的量是0.8mol;2mol He中原子的物质的量是2mol,因此所含原子个数从大到小的顺序为①>⑤>③>②>④。
;0.2 mol氨气(NH3)分子中含有的原子的物质的量是0.8mol;2mol He中原子的物质的量是2mol,因此所含原子个数从大到小的顺序为①>⑤>③>②>④。
(3)根据物质的量浓度与质量分数的关系可知![]() 、
、![]() ,硫酸溶液的浓度 越大,密度越大,则ρ1<ρ2,所以c1和c2的数值关系是2c1<c2。
,硫酸溶液的浓度 越大,密度越大,则ρ1<ρ2,所以c1和c2的数值关系是2c1<c2。
(4)恒温、恒容条件下,气体的压强之比等于其物质的量之比,一定量的元素A的氢化物AH3,在恒温密封容器中完全分解为两种气态单质,此时压强增加了75%,则反应前后压强之比=1:(1+75%)=4:7,同一化学反应中混合气体的物质的量之比等于其计量数之和的比,所以反应前后AH3与氢气和A物质的计量数之和之比为4:7,结合质量守恒定律得方程式为4AH3=6H2+A4。


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,将X溶液逐滴加入固体Y中,装置B的试管中的现象不正确的是( )
选项 | X溶液 | 固体Y | Z溶液 | 现象 |
|
A | 浓硫酸 | 亚硫酸氢钠 | 品红试液 | 品红褪色 | |
B | 浓氨水 | CaO | 紫色石蕊试液 | 溶液变红 | |
C | 盐酸 | 石灰石 | 硅酸钠溶液 | 出现白色沉淀 | |
D | 双氧水 | MnO2 | 氢硫酸溶液 | 产生浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活刀相关:下列有关说法
A. 用二氧化硫漂白后的食品显得白亮,二氧化硫可作食品漂白剂
B. 油脂在人体内水解为氨基酸和甘油等小分子物质后才能被吸收
C. “天官二号”中使用的碳纤维是一种新型无机非金属材料
D. 向牛奶中加入果汁会产生沉淀,这是因为酸碱发生了中和反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关工业合成氨的说法不能用平衡移动原理解释的是
A.不断补充氮气和氢气
B.选择20MPa-50MPa的高压
C.及时液化分离氨气
D.选择500℃左右同时使用铁触媒做催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
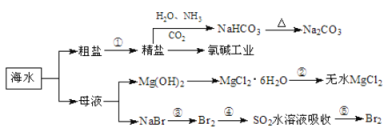
下列有关说法正确的是
A.在第③、④、⑤步骤中,溴元素均被氧化
B.制取NaHCO3的反应是利用其在此反应所涉及物质中溶解度最小
C.用澄清的石灰水可鉴别NaHCO3和Na2CO3
D.工业上通过电解饱和MgCl2溶液制取金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象得出的结论正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 将某溶液与稀盐酸反应产生的气体通入澄清石灰水 | 石灰水变浑浊 | 该溶液中一定含有CO |
B | 将干燥的Cl2通过有色鲜花 | 鲜花褪色 | Cl2有漂白性 |
C | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生气体 | Na2O2没有变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是几种常见的化学电源示意图,有关说法不正确的是

A. 上述电池分别属于一次电池、二次电池和燃料电池
B. 干电池在长时间使用后,锌筒被破坏
C. 铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
D. 氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)CO2是大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是:
2CO2(g) + 6H2(g)![]() CH3OCH3(g) + 3H2O(g) △H>0。
CH3OCH3(g) + 3H2O(g) △H>0。
①写出该反应的平衡常数表达式 。
②判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是 。
A.容器中密度不变
B.单位时间内消耗2molCO2,同时消耗1mol二甲醚
C.v(CO2)︰v(H2)=1︰3
D.容器内压强保持不变
(2)汽车尾气净化的主要原理为:2NO(g) + 2CO (g)![]() 2CO2 (g) + N2 (g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
2CO2 (g) + N2 (g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
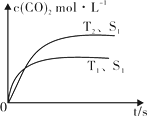
① 该反应的ΔH 0(选填“>”、“<”)。
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线。
(3)已知:CO(g) + 2H2(g)![]() CH3OH(g)△H = ﹣a kJmol-1。
CH3OH(g)△H = ﹣a kJmol-1。
①经测定不同温度下该反应的平衡常数如下:
温度(℃) | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4 mol·L-1、c(H2)=0.4 mol·L-1、c(CH3OH)=0.8 mol·L-1, 则此时v正 v逆(填“>”、“<”或“=”)。
②某温度下,在体积固定的2L的密闭容器中将1 mol CO和2 mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(P后/P前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
则前15分钟,用氢气表示的平均化学反应速率为 ,达到平衡时CO的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com