
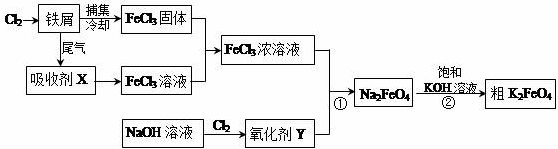
分析 氯气与铁反应生成三氯化铁,冷却得到三氯化铁固体,尾气中含有氯气,用氯化亚铁溶液吸收得到氯化铁溶液,把氯化铁固体溶于吸收液得到浓氯化铁溶液,氯气与氢氧化钠溶液反应生成次氯酸钠溶液,次氯酸钠具有强氧化性,与氯化铁溶液反应生成Na2FeO4,然后向该溶液中加饱和的KOH溶液,析出固体K2FeO4,
(1)①氯化铁做净水剂是因为Fe3+水为Fe(OH)3胶体的缘故;
②工业上常用FeCl3溶液腐蚀铜印刷线路板是Fe3+氧化了Cu的缘故;
(2)吸收剂X的与Cl2反应的产物是FeCl3,X是FeCl2;Cl2与氢氧化钠反应生成NaClO和NaCl,其中NaClO能做氧化剂;
(3)碱性条件下根据反应物和产物及元素守恒和电荷守恒可写出反应①的离子方程式;
(4)根据溶解度大小分析可知,在反应中溶解度小的物质先析出,会促进反应的进行;
(5)K2FeO4 在水溶液中易发生反应:4FeO42-+10H2O═4Fe(OH)3+8OH-+3O2↑,所以用碱液来洗涤,抑制水解,不引入新的杂质所以用稀KOH溶液,异丙醇易挥发;
(6)根据反应①②③可知:2FeO42-~~~~6Fe2+,根据关系式计算出K2FeO4的物质的量和质量,再计算质量分数.
解答 解:(1)①氯化铁做净水剂是因为Fe3+水为Fe(OH)3胶体的缘故,原理为Fe3++3H2O?Fe(OH)3(胶体)+3H+,
故答案为:Fe3++3H2O?Fe(OH)3(胶体)+3H+;
②工业上常用FeCl3溶液腐蚀铜印刷线路板,是Fe3+氧化了Cu的缘故,反应方程式为2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)吸收剂X的与Cl2反应的产物是FeCl3,X是FeCl2;Cl2与氢氧化钠反应生成NaClO和NaCl,其中NaClO能做氧化剂,所以Y为NaClO,
故答案为:FeCl2;NaClO;
(3)碱性条件下根据反应物和产物可知,反应①的离子方程式为3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O;
故答案为:3ClO-+2Fe3++10OH-=2FeO42-+3Cl-+5H2O;
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品,该反应的化学方程式为2KOH+Na2FeO4 =K2FeO4+2NaOH,反应能发生的原因是K2FeO4溶解度小,析出晶体,促进反应进行;
故答案为:K2FeO4溶解度小,析出晶体,促进反应进行;
(5)K2FeO4 在水溶液中易发生反应:4FeO42-+10H2O═4Fe(OH)3+8OH-+3O2↑,所以用碱液来洗涤,抑制水解,不引入新的杂质所以用稀KOH溶液,异丙醇易挥发,故选B;
(6)根据反应①②③可知:2FeO42-~~~~6Fe2+,
1mol 3mol
n 0.1000mol/L×0.01893L
则n=6.31×10-4mol,
所以样品中高铁酸钾的质量分数为$\frac{6.31×10{\;}^{-4}mol×\frac{250}{25}×198g/mol}{1.98g}$×100%=63.1%;
故答案为:63.1%.
点评 本题考查了物质的制备流程的理解应用、实验基本操作、物质性质的分析应用、有关方程式的计算、氧化还原反应等,题目涉及的知识点较多,侧重于考查学生的实验能力和对基础知识的综合应用能力,熟练掌握基础是关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸使胆矾晶体的蓝色褪去,说明浓硫酸具有吸水性 | |
| B. | 豆科植物根部的根瘤菌可以将空气中的氮由游离态转为化合态是氮的固定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 氨水可使酚酞试剂变为红色,说明氨水显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
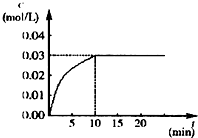 在某一容积为5L的密闭容器内,加入 0.2mol的CO和0.2mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0,反应中CO2的浓度随时间变化情况如图:
在某一容积为5L的密闭容器内,加入 0.2mol的CO和0.2mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),△H<0,反应中CO2的浓度随时间变化情况如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠与盐酸;氢氧化铜与盐酸 | B. | BaCl2与Na2SO4;Ba(OH)2与H2SO4 | ||
| C. | Na2CO3与硝酸;CaCO3与硝酸 | D. | 石灰石与硝酸反应;石灰石与盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ② | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaA的溶液呈碱性 | B. | pH=2的HA溶液稀释100倍后pH=3.5 | ||
| C. | 0.01 mol•Lˉ1HA溶液的pH=4 | D. | HA溶液跟锌反应,放出H2很慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2A+3B=2C | B. | A+3B2=C | C. | 3A+B=2C | D. | A+B=C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯水中c(H+)•c(OH-)=1×10-14 | B. | 25℃纯水中c(H+)•c(OH-)=1×10-14 | ||
| C. | 25℃稀盐酸中c(H+)•c(OH-)=1×10-14 | D. | KW值随温度升高而增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com