
����Ŀ�����طŵ�ʱ����ԭ��ص����ã��ڳ��ʱ����ص����ã���ʽ�ǰ��������طֱ��ڳ�硢�ŵ�ʱ�ķ�Ӧ��Fe+NiO2+2H2O ![]() Fe��OH��2+Ni��OH��2 �� �����йذ�������صĸ����ƶ��д�����ǣ� ��
Fe��OH��2+Ni��OH��2 �� �����йذ�������صĸ����ƶ��д�����ǣ� ��
A.�ŵ�ʱ����������NiO2������
B.���ʱ�����ϵĵ缫��ӦΪ��Fe��OH��2+2e���TFe+2OH��
C.�ŵ�ʱ���������Һ�е��������������������ƶ�
D.���ص������缫��������ڼ�����Һ��
���𰸡�C
���������⣺A���ŵ�ʱ��ԭ��أ�������Fe��2e��+2OH��=Fe��OH��2 �� ������NiO2+2e��+2H2O=Ni��OH��2+2OH�� �� ��A��ȷ�� B������ǵ��أ��ɷ���ʽ��֪�˵��Ϊ���Ե�أ���Ӧ����ʽʱ���ܳ���H+ �� ���Գ��ʱ�����������ĵ缫��Ӧʽ�ͷֱ�Ϊ��Fe��OH��2+2e��=Fe+2OH����2Ni��OH��2+2OH����2e��=Ni2O3+3H2O����B��ȷ��
C���ŵ�ʱ��ԭ��أ�������Fe��2e��+2OH��=Fe��OH��2 �� ������NiO2+2e��+2H2O=Ni��OH��2+2OH�� �� �������Һ�е��������������ƶ�����C����
D���ɷ���ʽ��֪�˵��Ϊ���Ե�أ�FE�ܹ����ᷴӦ���������صĵ缫���ڼ��Ե������Һ�У���D��ȷ��
��ѡC��


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ע���ķ����������и���������в���ȷ���ǣ� ��
A. ������������Һ������ B. ʳ���е�ɳ�����ܽ���ˣ�
C. �������������ˮ�����ˣ� D. �����ͺ�ˮ����Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����طŵ�ʱ����ԭ��ص����ã��ڳ��ʱ����ص����ã���ʽ�ǰ��������طֱ��ڳ�硢�ŵ�ʱ�ķ�Ӧ��Fe+NiO2+2H2O ![]() Fe��OH��2+Ni��OH��2 �� �����йذ�������صĸ����ƶ��д�����ǣ� ��
Fe��OH��2+Ni��OH��2 �� �����йذ�������صĸ����ƶ��д�����ǣ� ��
A.�ŵ�ʱ����������NiO2������
B.���ʱ�����ϵĵ缫��ӦΪ��Fe��OH��2+2e���TFe+2OH��
C.�ŵ�ʱ���������Һ�е��������������������ƶ�
D.���ص������缫��������ڼ�����Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͬ��ͬѹ�µ������CO2��CO����������������� ���ܶ���� ��������������� ������ԭ�Ӹ�����ȣ�������ȷ���ǣ� ��
A. �� B. �ڢۢ� C. �ۢ� D. �٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ΪԤ���Ϳ��Ƹ�Ѫѹ��WHO����ÿ��ÿ��ʳ��������Ӧ���� 6g������������ȷ���� ( )
A. �Ȼ�����Һ�ڵ��������µ����Na+��Cl-
B. ij���������ǵ���ʣ���һ���Ƿǵ����
C. ���ᱵ������ˮ�������ᱵ�ǵ����
D. ������̼��ˮ��Һ�ܵ��磬�ʶ�����̼���ڵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧѧϰС���ڰ�����ʦ����ʵ���ҵĻ�ѧ�Լ�ʱ������һƿ��ɫ��Һ����ǩ��������ͼ������ʦ���䣬��ҩƷӦ������ѧ��ѧ�����Լ�����С��ͬѧ���������յ�֪ʶ������Һ���м���������˵���������
A. ��С��ͬѧ�Ʋ����������ӿ�����H+��Na+��K+��NH4+�е�ijһ��
B. ��Ҫ֤���������Ƿ�ΪNH4+,�䷽����: ȡ������Һ���Թ��м�ϡNaOH��Һ����������ʹʪ��ĺ�ɫʯ����ֽ���������壬��������ΪNH4+
C. ijͬѧ����ʱ������һ����Һ������ֽ�ϣ�ֽ��ڣ�˵������ҺΪŨ����
D. ��֤�������Ƿ�ΪNa+����K+��ʵ�鷽������ɫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ϊ����������ͭ��Ӧ��������Ⱦ�����Թ�ҵ�ϳ��ð�����ԭ����ͭ��ȡͭ��������ѧ��ѧ��ȤС��Ϊ��ģ��÷�Ӧ��ͬʱ���ͭ�����ԭ�������IJⶨ�����������ʾ��װ��ͼ��������ʵ��:
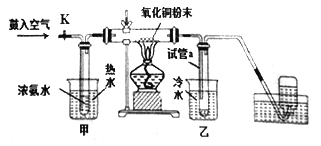
�ٶ����ⶨͭ�����ԭ��������ʵ������У�����ͭ��ַ�Ӧ�����������������
A. �ر�K����������ʵ�飬����Թ������ռ�����Һ������������ͭ�������������ͭ�����ԭ������
B. �ر�K����������ʵ�飬�������ͭ�ķ�ĩ�ķ�Ӧǰ������������ռ���ƿ���ռ������������(��״����)�������ͭ�����ԭ������
C. ֱ�Ͳ������з����ķ�ӦΪ��3CuO+2NH3![]() N2��+3Cu+3H2O
N2��+3Cu+3H2O
D. ����K�����������ֱ�Ͳ�����������ͭ��ĩ�ύ����ֺ�ɫ���ɫ����ɫ���ɫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ӵ�ʳ����ͨ���������KIO3 �� �����������������±��ֳ���ǿ�������ԣ����Ժ͵⻯��������εȻ�ԭ�����ʷ�����Ӧ��
��1��д��KIO3��KI��ϡ��������з�����Ӧ�����ӷ���ʽ
��2��Ϊ�ⶨ�˼ӵ����е�Ԫ�صĺ�����ijѧ�������������ʵ�飺 A��ȷ��ȡw gʳ�Σ�ʹ����ȫ�ܽ�������������ˮ�У�
B����ϡ�����ữ������Һ�����������KI��Һ��ʹ���ַ�Ӧ��
C����Ϊָʾ������μ������ʵ���Ũ��Ϊ2.0��10��3mol/L�������������Һ10.0mL��ǡ����ȫ��Ӧ���жϷ�Ӧ��ȫ��ʵ������Ϊ �� ��üӵ�����Ʒ�е�Ԫ�صĺ���Ϊmg/Kg���ú�w�Ĵ���ʽ��ʾ����
����֪��I2+2S2O32���T2I��+S4O62����
��3��ijѧ�����ֽ���������ʵ�飺 A��ȷ��ȡ1.0g������NaCl����3mL����ˮ�����Һ����ҺΪ��ɫ��
B������5��ָʾ����1mL 0��lmol/L KI��Һ���������Һ���仯��
C�������μ�l��1mol/L��������Һ���������Һ����ɫ
�Ʋ�ʵ���в�����ɫ�����ԭ�������ӷ���ʽ��ʾ
����ѧ���ҵ�ʵ���������ѧ����ʵ�������з���ƫ��ƫС����ȷ������ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. Na+��Ħ��������23
B. 1mol O2������Ϊ32g/mol
C. ��ԭ�ӵ�Ħ�����������������ԭ������
D. H2SO4��Ħ��������98g/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com