
 的同分异构体甚多,其中属于酯类化合物而且结构中有苯环结构的同分异构体就有6种,它们是:
的同分异构体甚多,其中属于酯类化合物而且结构中有苯环结构的同分异构体就有6种,它们是:


 .
. 分析 本题有两个限制条件:属于酯类化合物且结构式中有苯环,不涉及类别异构.由酯的组成可知: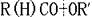 ,虚线左侧来源于酸,右侧来源于醇.将它转化为3种酰基:HCO-、CH3CO-、
,虚线左侧来源于酸,右侧来源于醇.将它转化为3种酰基:HCO-、CH3CO-、 ;6种烃氧基:
;6种烃氧基: 、
、 、
、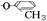 、
、 、
、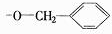 、
、 .根据其组成,两两相接,可写出6种酯的结构.
.根据其组成,两两相接,可写出6种酯的结构.
解答 解: 的分子式为C8H8O2 ,除去苯环的6个碳原子,还有2个碳原子去形成酯的结构,这些酯的同分异构体有:乙酸苯酚酯(1种);甲酸甲苯酚酯(3种):甲酸苯甲酯(1种);苯甲酸甲酯(1种). 因此,含有苯环结构并属于酯类化合物的同分异构体有:
的分子式为C8H8O2 ,除去苯环的6个碳原子,还有2个碳原子去形成酯的结构,这些酯的同分异构体有:乙酸苯酚酯(1种);甲酸甲苯酚酯(3种):甲酸苯甲酯(1种);苯甲酸甲酯(1种). 因此,含有苯环结构并属于酯类化合物的同分异构体有: ;
; ;
; ;
;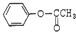 ;
;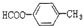 ;
; ;
;
故答案为: ;
; ;
;
点评 本题考查限制条件下同分异构体的书写,掌握有机物的官能团和结构为解答该题的关键,难度中等.


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:多选题
| A. | 乙烯的结构简式CH2CH2 | B. | 乙醇的分子式C2H6O | ||
| C. | 乙酸乙脂的结构简式是CH3COOC2H5 | D. | 四氯化碳的电子式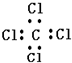 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
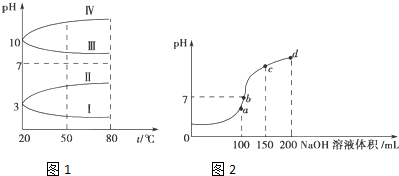
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、丙炔 | B. | 甲醛、果糖 | C. | 乙醇、乙二醇 | D. | 甲苯、甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论 | |
| A | 向某未知溶液中加入盐酸酸化的BaCl2溶液 | 生成白色沉淀 | 该溶液中一定含有SO42- |
| B | 用一束强光照射Na2SiO3溶液 | 溶液中出现一条光亮的通路 | 溶液中可能含有硅酸胶体 |
| C | 向盛有Fe(NO3)2溶液的试管中滴入几滴0.1mol/LH2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| D | 淀粉溶液中加稀硫酸,加热片刻后再滴加银氨溶液,并用水浴加热 | 无银镜生成 | 淀粉未发生水解 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
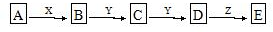
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜粉放入硝酸银溶液里:Cu+Ag+═Cu2++Ag | |
| B. | 铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 澄清石灰水与稀盐酸反应:OH-+H+═H2O | |
| D. | 硫酸铜溶液和氢氧化钠溶液反应:CuSO4+2OH-═Cu(OH)2↓+SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com