
| Ⅰ | A、B、C、D、E、F、G七种短周期元素的原子序数依次增大 |
| Ⅱ | A和E同主族,B和F同主族,D和G同主族 |
| Ⅲ | A原子核内只有质子没有中子,B原子最外层电子数是电子层数的2倍 |
| Ⅳ | D和F以原子个数比为2:1组成的物质X是光导纤维的主要成分 |
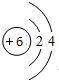 ,物质X的化学式为SiO2
,物质X的化学式为SiO2分析 A、B、C、D、E、F、G七种短周期元素的原子序数依次增大,A和E同主族,A原子核内只有质子没有中子,则A为H元素,则E为Na,D和F以原子个数比为2:1组成的物质X是光导纤维的主要成分,则X为SiO2,所以D为O,F为Si,D和G同主族,则G为S,B原子最外层电子数是电子层数的2倍,则B为C或S元素,B和F同主族,则B为C,C的原子序数介于B、D之间,所以C为N,据此答题.
解答 解:A、B、C、D、E、F、G七种短周期元素的原子序数依次增大,A和E同主族,A原子核内只有质子没有中子,则A为H元素,则E为Na,D和F以原子个数比为2:1组成的物质X是光导纤维的主要成分,则X为SiO2,所以D为O,F为Si,D和G同主族,则G为S,B原子最外层电子数是电子层数的2倍,则B为C或S元素,B和F同主族,则B为C,C的原子序数介于B、D之间,所以C为N,
(1)B为C,B的原子结构示意图为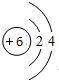 ,物质X的化学式为SiO2,
,物质X的化学式为SiO2,
故答案为: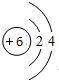 ;SiO2;
;SiO2;
(2)C为N,D为O,F为Si,元素地非金属性越强,氢化物越稳定,非金属性O>N>Si,所以三种元素对应的氢化物稳定性大小顺序是H2O>NH3>SiH4,
故答案为:H2O>NH3>SiH4;
(3)A、D、E三种元素形成的化合物为氢氧化钠,其中存在的化学键类型是离子键、共价键,
故答案为:离子键、共价键;
(4)有两种盐,它们均由A、D、E、G四种元素组成,这两种盐为硫酸氢钠和亚硫酸氢钠,二者在溶液中反应的离子方程式是H++HSO3-=SO2↑+H2O,
故答案为:H++HSO3-=SO2↑+H2O;
(5)同主族元素,从下向下非金属性增强,所以C、Si两元素中非金属性较强的是碳,根据元素最高价氧化物水化物的酸性强弱证明非金属性强弱,实验为:取硅酸钠溶液于试管中,向其中通入二氧化碳气体,观察是否有白色沉淀产生,
故答案为:碳;取硅酸钠溶液于试管中,向其中通入二氧化碳气体,观察是否有白色沉淀产生.
点评 本题考查了位置性质结构的关系及应用,正确推断元素是解本题关键,根据原子结构和元素周期律等知识点来分析解答,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 在体积均为1.0L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
在体积均为1.0L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )| A. | 状态Ⅱ和状态ⅢCO2的转化率相同 | |
| B. | 体系的总压强PⅢ:P总(状态Ⅱ)>2PⅠ (状态Ⅰ) | |
| C. | 反应的平衡常数:KⅠ>KⅡ=KⅢ | |
| D. | 逆反应速率v逆:v逆(状态Ⅰ)>v逆(状态Ⅲ) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 两极材料 | Zn片、石墨 | Zn片、Cu片 | Cu片、Ag片 | Fe片、Cu片 |
| 插入溶液 | CuSO4溶液 | 无水酒精 | AgNO3溶液 | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性强弱:H2SiO3<H2CO3<H2SO4 | B. | 热稳定性:HCl>HBr>HI | ||
| C. | 原子半径:Na<Mg<Al | D. | 熔点:SiO2>NaCl>CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B60和C90都属于新型化合物 | B. | C60和N60属于同分异构体 | ||
| C. | B60、C60、C90、N60都只含共价键 | D. | B60、C60、C90、N60都属于烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铝的熔点很低,不能用于制作耐高温材料 | |
| B. | 光化学烟雾与大量排放碳氢化合物和氮氧化合物有关 | |
| C. | 无水乙醇用作医用消毒剂效果更好 | |
| D. | Na、S、C分别在氧气中点燃均可得到两种不同的氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的氧化剂是水 | |
| B. | 该反应的还原剂是水 | |
| C. | 氧化剂和还原剂的物质的量比为1:2 | |
| D. | 若有3molNO2反应,则转移电子4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LCO2的质量为22g | |
| B. | 0.1molCl2与足量水反应转移电子0.2mol | |
| C. | 18gH2O含有的原子总数为3×6.02×1023 | |
| D. | 0.5mol/L Na2SO3溶液中Na+的物质的量浓度为1.0 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com