
【题目】已知A~K均为中学化学中的常见物质,它们之间的转化关系如下图所示,其中A、D为金属单质,反应过程中生成的水及其他部分产物已略去。
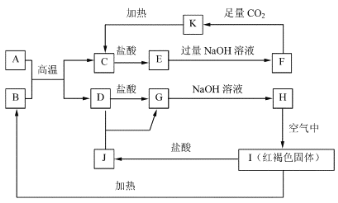
请回答以下问题:
(1)C________H________F (填化学式)
(2)A与B在高温下反应的化学方程式为 。
(3)H变成I的化学方程式是 。
(4)向F中通入足量CO2生成K的离子方程式为 。
(5)D+J生成G的离子方程式为 。
[
【答案】(11分)
(1)C Al2O3 H Fe(OH)2 F NaAlO2 (3分)
(2)2Al+Fe2O3![]() Al2O3+2Fe (2分)
Al2O3+2Fe (2分)
(3)4Fe(OH)2+O2+2H2O==4Fe(OH)3 (2分)
(4)CO2+AlO2-+2H2O==Al(OH)3 ↓+HCO3- (2分)
(5)2Fe3++Fe==3Fe2+ (2分)
【解析】
试题分析:I为红褐色固体,则I为Fe(OH)3;依据转化关系中的现象分析判断,H为Fe(OH)2;氢氧化铁加热生成的B为Fe2O3,依据J是氢氧化铁和盐酸反应生成的氯化铁,判断D为铁,G为FeCl2,依据A+B在高温下反应判断,A为Al,D为Fe,C为Al2O3,K加热生成氧化铝,说明K为Al(OH)3,E为AlCl3,F为NaAlO2;由此分析可知:
(1)C为Al2O3,H为Fe(OH)2,F为NaAlO2,故答案为:C: Al2O3,H:Fe(OH)2,F: NaAlO2;
(2)A为Al,B为Fe2O3,A与B在高温下反应的化学方程式为:2Al+Fe2O3![]() Al2O3+2Fe;
Al2O3+2Fe;
(3)Fe(OH)2变成Fe(OH)3的化学方程式是:4Fe(OH)2+O2+2H2O==4Fe(OH)3;
(4)向 NaAlO2中通入足量CO2生成Al(OH)3的离子方程式为CO2+AlO2-+2H2O==Al(OH)3↓+HCO3-;
(5)D+J生成G的离子方程式为2Fe3++Fe==3Fe2+


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。比如:

(1)上图所示的物质分类方法名称是 ;
(2)按上述分类法,下列物质中Fe、O2、H2SO4、Ba(OH)2、Ca(HCO3)2、SO2属于酸的是__________,这些物质间有的可发生化学反应,请写出一个属于置换反应的离子方程式:___________________;
人们利用分类法对化学物质和化学反应进行分类学习,例如CO2属于二元弱酸的酸性氧化物,Ca(OH)2属于强碱,已知将过量CO2缓缓通入澄清石灰水中,溶液先变浑浊,后又变澄清;NaOH也属于强碱,请写出:
少量CO2与NaOH溶液反应的离子方程式:____________________________;
过量CO2与NaOH溶液反应的离子方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可持续进行,直至反应完全生成新物质硫化亚铁。这现象说明了( )
A.该反应是吸热反应 B.铁粉和硫粉在常温下可以发生反应
C.该反应是放热反应 D.硫化亚铁的总能量高于铁粉和硫粉的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.10g镁铝合金加入120mL4.0mol·L-1的盐酸中,待合金完全溶解后,得到溶液X。下列说法一定正确的是
A. 合金完全溶解后产生的H2的物质的量为0.24mol
B. 合金中的镁与铝的物质的量之比小于1
C. 若向溶液X中加入270mL2.0mol·L-1NaOH溶液,充分反应,所得沉淀为Mg(OH)2
D. 若向溶液X中加入足量的氨水,充分反应,所得沉淀经过过滤、洗涤后充分灼烧,则残留固体质量大于8.50g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是 ( )
A. 在催化剂存在条件下苯与液溴反应制溴苯
B. 苯与浓硝酸、浓硫酸混合共热制取硝基苯
C. 苯与浓硫酸共热制取苯磺酸
D. 在一定条件下苯与氢气反应制环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列溶液中,各组离子一定能够大量共存的是
A.使酚酞试液变红的溶液:Na+、Cl-、SO![]() 、Fe3+
、Fe3+
B.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、MnO![]() 、Cl-
、Cl-
C.pH<7的溶液:K+、Ba2+、Cl-、Br-
D.碳酸氢钠溶液:K+、SO![]() 、Cl-、H+
、Cl-、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g)![]() 2NH3(g)ΔH=-92.4kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g)ΔH=-92.4kJ·mol-1。一种工业合成氨的简式流程图如下:
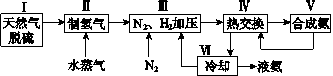
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:_______________________。
(2)步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g)△H=+206.4kJ·mol-1
CO(g)+3H2(g)△H=+206.4kJ·mol-1
②CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=-41.2kJ·mol-1
CO2(g)+H2(g)△H=-41.2kJ·mol-1
对于反应①,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是____________。
a.升高温度b.增大水蒸气浓度c.加入催化剂d.降低压强
利用反应②,将CO进一步转化,可提高H2的产量。若1molCO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO的转化率为__________。
(3)图(a)表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:____________。
(4)依据温度对合成氨反应的影响,在图(b)坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。
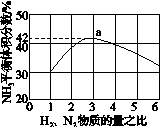
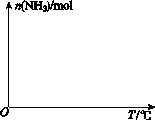
(a)(b)
(5)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)________。简述本流程中提高合成氨原料总转化率的方法:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能大量共存的是 ( )
A.K+、HCO3-、CO32-、Br- B.SO32-、HSO3-、OH-、K+
C.Fe3+、Cu2+、NO3-、SO32- D.H+、Na+、NO3-、Fe2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com