
【题目】我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表),经X射线衍射测得R的局部结构如图所示,下列说法正确的是( )
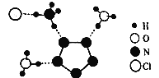
A.R中两种阳离子的中心原子的杂化轨道类型相同,但化学键类型不同
B.1molR中σ键总数为15个
C.N5-中参与形成的大π键电子数为6个
D.已知图中虚线代表氢键,其中一个表示为(NH4)N﹣H···Cl,则化合物R中共有4个不同类型氢键
【答案】C
【解析】
A.R中阳离子为NH4+中心原子为sp3杂化轨道,形成3个σ键和1个配位键,另一种阳离子为H3O+,中心原子为sp3杂化轨道,形成2个σ键和1个配位键键,所以二者中心原子的杂化轨道类型相同,化学键类型相同,故A错误;
B.据图可知1molR中σ键总数为15NA,故B错误;
C.N5-中每个N形成两条共价键,pz轨道留有一个单电子,5个N的5个pz轨道交盖形成离域大π键;N5-的价电子总数为5×5+1=26,σ键个数为5,每个氮原子有1对孤电子对,且未参与形成大π键,所以参与形成大π键的电子数为26-5×2-5×2=6,故C正确;
D.据图可知除(NH4+)N-H···Cl外还有(H3O+)O-H···N(N5-)、(NH4+)N-H···N(N5-)两种氢键,共三种,故D错误;
故答案为C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】根据下列实验操作回答有关问题:
(1)在盛有![]() 溶液的试管中逐滴滴加少量的
溶液的试管中逐滴滴加少量的![]() 溶液,可观察到的现象是______,该反应的离子方程式为______。
溶液,可观察到的现象是______,该反应的离子方程式为______。
(2)将(1)中所得的混合物平均分成两分,向其中一份中继续滴加![]() 溶液,直至过量,现象是______,反应的离子方程式为______;向另一份中加入足量稀硫酸,现象是______,反应的离子方程式为______。
溶液,直至过量,现象是______,反应的离子方程式为______;向另一份中加入足量稀硫酸,现象是______,反应的离子方程式为______。
(3)(2)中反应说明![]() 所属的物质类别是______。
所属的物质类别是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液 X,可能含有 Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,其现象及转化如下图。反应过程中有一种气体是红棕色。请回答下列问题:
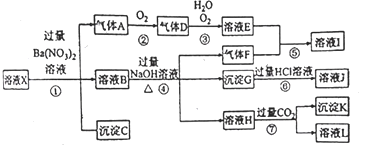
(1)由强酸性条件即可判断溶液X中一定不存在的离子有___________________。
(2)溶液X中,关于NO3-的判断一定正确的是___________。
a.一定有 b.一定没有 c.可能有
(3)产生气体A的离子方程式为________________ ,并用双线桥法表示电子转移的方向和数目。
(4)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,则反应中D与O2的物质的量之比为__________。
(5)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的—种,根据现象即可判断,该试剂最好是_____________ 。
①NaOH溶液 ②KSCN溶液 ③石蕊试剂 ④pH试纸 ⑤KMnO4溶液⑥氯水和KSCN的混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校科学活动小组对教材中“测定空气里氧气含量”的实验(如图1)进行了大胆改进,设计如图2(选用容积为40mL的试管作为反应容器和润滑性很好的注射器组装)实验方案进行。请你对比分析图1、图2实验,回答下列有关问题:

I.请结合图1回答下列问题:
(1)指出实验中A、B仪器的名称:A___;B___。
(2)写出红磷燃烧反应的表达式___。
(3)实验中点燃红磷后观察到___,待红磷熄灭并冷却至室温后,打开弹簧夹,观察到___。
(4)由此实验可推知剩余主要气体的化学性质是___(答一条即可)。
II.改用图2实验方案进行,实验的操作步骤如下:①将红磷装入试管中,将30mL的注射器活塞置于10mL刻度处,并按图2中所示的连接方式固定好,再将弹簧夹夹紧橡皮管②点燃酒精灯③撤去酒精灯,待试管冷却后松开弹簧夹④读取注射器活塞的数据。
(5)与图1比较,图2装置的优点是___(答一点即可)。
(6)若用图2装置测得的氧气体积分数小于![]() ,则可能的原因是___(写一条即可)。
,则可能的原因是___(写一条即可)。
(7)图2实验中注射器活塞将从10mL刻度处慢慢前移到约为___mL刻度处才停止(忽略导管气体体积)。
(8)若图2装置中改用容积为80mL试管且不使用夹弹簧夹,其它操作都不变,为确保实验成功,则加热前注射器活塞前沿至少应调整到___mL刻度处(填整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬烯在食品中作为香料添加剂被广泛使用,其结构简式为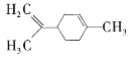 。下列有关柠檬烯的分析正确的是( )
。下列有关柠檬烯的分析正确的是( )
A.1mol柠檬烯完全燃烧消耗14molO2
B.分子中所有碳原子可能在同一平面上
C.和丁基苯(![]() )互为同分异构体
)互为同分异构体
D.一定条件下,可以发生加成反应、取代反应、氧化反应、酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。

(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是__________。
②称取样品,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为________、________。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是_______________。
②E处干燥管中盛放的药品是碱石灰,其作用是_____________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量_____________(填“偏大”“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m1g、m2g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成气态分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同电子数,且D是同周期元素中原子半径最大的元素;E元素的原子最外层比次外层少两个电子,C、F两种元素的原子最外层共有13个电子。则
(1)X的化学名称为__________。
(2)B单质的结构式为__________;E的气态氢化物的电子式为__________;C与D形成的两种化合物中,其中一种物质含有两种类型的化学键,分别为______________,该物质属于______________(填“离子化合物”或“共价化合物”)。
(3)B、C、E分别与A形成的化合物中最稳定的是__________(写化学式)。
(4)D是同周期简单阳离子中离子半径最__________(填“大”或“小”)的元素。
(5)F的单质在反应中常作________剂(填“氧化”或“还原”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
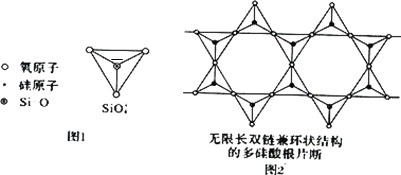
【题目】(1)某物质的晶体内部一个截面上原子的排布情况如图所示,则该晶体的化学式可表示为________
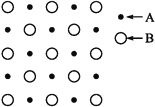
(2)Si 元素以 Si-O-Si 链构成矿物界,由许多四面体(图 l)连接成无限长的单链或双链(图 2)结构。图 2 所示的多硅酸根离子的化学式通式为________(以含正整数 n 的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,同时发生反应A(g)![]() B(g)和A(g)
B(g)和A(g)![]() C(g)。已知A(g)反应生成B(g)或C(g)的能量如图所示,下列说法正确的是
C(g)。已知A(g)反应生成B(g)或C(g)的能量如图所示,下列说法正确的是
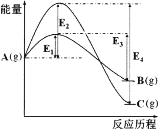
A.B(g)比C(g)稳定
B.在该温度下,反应刚开始时,产物以B为主;反应足够长时间,产物以C为主
C.反应A(g![]() )B(g)的活化能为(E3—E1)
)B(g)的活化能为(E3—E1)
D.反应A(g)![]() C(g)的ΔH<0且ΔS=0
C(g)的ΔH<0且ΔS=0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com