
【题目】(化学——选修3:物质结构与性质)
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是__________________。
(2)A、B、C 三种元素的氢化物稳定性由强到弱的顺序为_________(用化学式表示)。
(3)A的最简单氢化物分子的空间构型为_______,其中A原子的杂化类型是________。
(4)A的单质中δ键的个数为_______________,π键的个数为_______________。
(5)写出基态E原子的价电子排布式:__________________________。
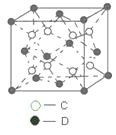
(6)C和D形成的化合物的晶胞结构如图所示,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a =________cm。(用ρ、NA的计算式表示)
【答案】H2O分子间存在氢键 HF>H2O >NH3 三角锥形 sp3 1 2 3d104s1 
【解析】
根据题给信息推断A为氮元素,B为氧元素,C为氟元素,D为钙元素,E为铜元素。
(1)B为氧元素,水的沸点是同族元素氢化物中最高的,原因是H2O分子间存在氢键。
(2)同周期元素由左向右元素的非金属性逐渐增强,气态氢化物的稳定性逐渐增强,故N、O、F 三种元素的氢化物稳定性由强到弱的顺序为HF>H2O >NH3。
(3)NH3中氮原子采取sp3杂化,含有1对孤对电子,分子的空间构型为三角锥形。
(4)两个成键原子间有且只有一个δ键,故N2分子含有氮氮三键,含有的δ键的个数为1,π键的个数为2。
(5)铜为29号元素,根据构造原理知基态铜原子的价电子排布式:3d104s1。
(6)C为氟元素,D为钙元素,根据CaF2晶胞结构利用切割法计算1个晶胞中含有8个F—,含有(8×1/8+6×1/2)=4个钙离子,故1mol晶胞的质量为4mol×78g/mol=312g,则ρ=312g/NAa3cm-3,晶胞
边长a = cm。
cm。


科目:高中化学 来源: 题型:
【题目】![]() 与
与![]()
![]() 的盐酸反应(放热反应)生成
的盐酸反应(放热反应)生成![]() 的量与反应时间的关系如图所示,下列结论不正确的是( )
的量与反应时间的关系如图所示,下列结论不正确的是( )
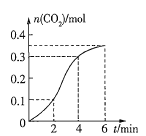
A.反应开始2min内平均反应速率最大
B.反应速率先增大后减小
C.2~4min内温度对反应速率的影响较大
D.反应在2~4min内生成![]() 的平均反应速率为
的平均反应速率为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某元素原子共有3个价电子,其中一个价电子位于第三能层![]() 能级,该能层有______个原子轨道,该元素基态原子的价电子排布图为______。
能级,该能层有______个原子轨道,该元素基态原子的价电子排布图为______。
(2)![]() 、
、![]() 均为短周期金属元素。依据下表数据,写出
均为短周期金属元素。依据下表数据,写出![]() 原子的核外电子排布式:______。
原子的核外电子排布式:______。
电离能/ |
|
|
|
|
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完成了如下实验:

已知:控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。
该同学得出的结论正确的是
A. 根据现象1可推出该试液中含有Na+
B. 根据现象2可推出该试液中并不含有葡萄糖酸根
C. 根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+
D. 根据现象5可推出该试液中一定含有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图串联装置中,通电片刻即发现乙装置左侧电极表面出现红色固体,则下列说法错误的是
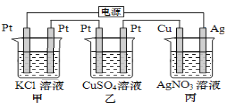
A.当丙中Cu电极质量增加21.6g,甲中共产生4.48 L气体
B.电解过程中丙中溶液pH无变化
C.向甲中加入适量的盐酸,可使溶液恢复到电解前的状态
D.乙中左侧电极反应式:Cu2++2e-=Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现将1.92gCu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL的NOX混合气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入标准状况下的O2的体积为( )
A. 504mLB. 336mLC. 224mLD. 168mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是425℃时,在1 L密闭容器中发生化学反应的浓度随时间的变化示意图。
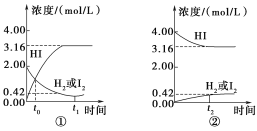
下列叙述错误的是( )
A. 图①中t0时,三种物质的物质的量相同
B. 图①中t0时,反应达到平衡状态
C. 图②中的可逆反应为2HI(g) ![]() H2(g)+I2(g)
H2(g)+I2(g)
D. 图①②中当c(HI)=3.16 mol/L时,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置进行乙醇氧化反应的探究实验,有关说法不正确的是()
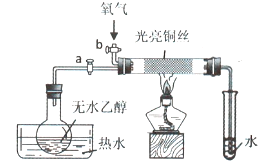
A.热水的作用是促使乙醇挥发,为硬质玻璃管内提供乙醇蒸汽
B.通入乙醇蒸汽反应的过程中,撤离酒精灯后反应仍能进行
C.在硬质玻璃管内发生的主反应为:![]()
D.实验结束时,先停止加热,再关闭活塞a、b,最后将导管移出水面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在钨酸盐催化作用下,以马来酸酐为原料,双氧水为氧化剂可合成环氧琥珀酸。马来酸酐转化率和环氧琥珀酸选择性随温度和催化剂用量的变化如图所示(保持其他条件相同)。下列说法不正确的是( )
![]()
![]()
![]()
![]()
![]()
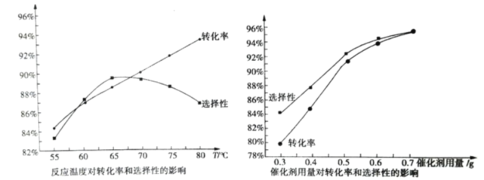
A.环氧琥珀酸的选择性随催化剂用量的增加而增加,故催化剂用量越多越好
B.当温度低于 65℃时,环氧琥珀酸的选择性随温度升高而增大
C.升高到一定温度后环氧琥珀酸的选择性降低,原因可能是环氧琥珀酸发生了水解反应
D.本实验适宜的反应温度为 65℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com