
| A、1.25 mol?L-1 |
| B、2.5 mol?L-1 |
| C、0.50 mol?L-1 |
| D、1.0 mol?L-1 |
| 8.4 |
| 22.4 |
| 0.25mol |
| 0.5L |


科目:高中化学 来源: 题型:
| A、常温下,1 mol 铁放入足量的浓硫酸中转移的电子数为0 | ||
B、标准状况下,密度为ρg?L-1的某气体纯净物一个分子的质量为
| ||
| C、将1mol Cl2通入到水中,得到的氯水中,N(HClO)+N(Cl-)+N(ClO-)<2NA | ||
| D、在含有4mol Si-O键的石英晶体中,氧原子的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=13的溶液:Cu2+、NH4+、NO3-、SO42- |
| B、含0.1 mol/L Fe3+的溶液:NH4+、Na+、Cl-、SO32- |
| C、滴入甲基橙试剂变红色的溶液:Na+、K+、AlO2-、SO42- |
| D、c(H+)=10-13 mol?L-1的溶液:K+、Na+、CO32-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
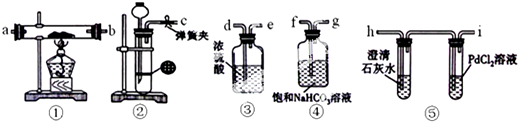
 在实验室中,制得纯净的气体,往往需要对气体进行干燥,某同学用如图所示装置干燥铁粉与水蒸气在高温条件下反应所得的H2,在干燥管中加入CaO固体,干燥后的H2点不燃,通过测定,发现是CaO固体变质导致的.
在实验室中,制得纯净的气体,往往需要对气体进行干燥,某同学用如图所示装置干燥铁粉与水蒸气在高温条件下反应所得的H2,在干燥管中加入CaO固体,干燥后的H2点不燃,通过测定,发现是CaO固体变质导致的.查看答案和解析>>
科目:高中化学 来源: 题型:
 对叔丁基苯酚
对叔丁基苯酚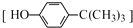 可用于生产油溶性酚醛树脂等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
可用于生产油溶性酚醛树脂等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下: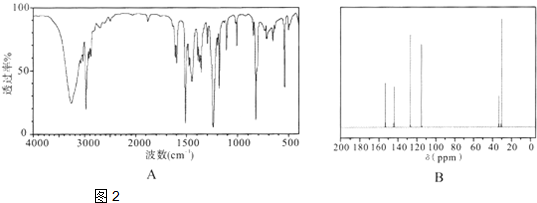
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O3+2KI+H2O═2KOH+I2+O2 |
| B、2CH3COOH+Ca(CIO)2═2HClO+(CH3COO)2Ca |
| C、I2+2NaClO3═2NalO3+Cl2 |
| D、4HCl(浓)+MnO2═MnCl2+Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 原因解释 |
| A | 将一片较簿的铝片放在酒精灯火焰上灼烧 | 铝片慢慢熔化呈液滴状 | 铝表面的氧化膜致密且熔点很高,阻碍铝与氧气的接触,同时铝的熔点较低熔化了 |
| B | 将等表面积的镁条、铝 片(均除去氧化膜)分 别放入装有等浓度、等 体积盐酸的两支试管中 | 都产生气泡,镁条表面产生气泡更快 | 镁的金属性比铝的金属性强,镁更易失去电子,所以反应更快 |
| C | 在打磨过的铁片上先滴 一滴饱和食盐水,再滴 一滴酚酞 | 液滴的外圈先出现红色 | 铁片不纯含有碳元素,铁、碳与食盐水形成原电池,溶液外圈发生吸氧腐蚀,导致c(OH-)增大,溶液呈碱性 |
| D | 取少量淀粉加稀硫酸, 加热几分钟,冷却后加 入新制氢氧化铜悬浊 液,加热至沸腾 | 未见砖红色沉淀生成 | 淀粉水解后没有葡萄糖生成 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com