
【题目】据最近报道,中国生产的首艘国产航母“山东”号已经下水。为保护航母、延长服役寿命可采用两种电化学方法。方法1:舰体镶嵌一些金属块;方法2:航母舰体与电源相连。下列有关说法正确的是( )
A. 方法1叫外加电流的阴极保护法
B. 方法2叫牺牲阳极的阴极保护法
C. 方法1中金属块可能是锌、锡和铜
D. 方法2中舰体连接电源的负极
科目:高中化学 来源: 题型:
【题目】相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。
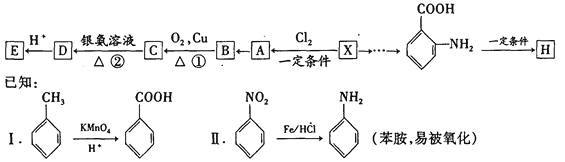
请根据所学知识与本题所给信息回答下列问题:
(1)X的名称为____________, B中官能团为____________。
(2)反应①的反应类型是____________
(3)H的结构简式是____________。
(4)反应②的化学方程式是____________。
(5) E有多种同分异构体,其中能发生银镜反应的芳香族化合物共有____种(不含立体异构),写出在核磁共振氢谱中能出现四组峰且其峰面积之比为l:1:2:2的同分异构体的结构简式为____________。
(6)请用合成流程图表示出由X和其他无机物合成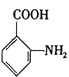 最合理的方案____________(不超过3步)。
最合理的方案____________(不超过3步)。
例: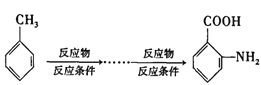
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝分别与足量的稀盐酸和氢氧化钠溶液反应时,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的盐酸和氢氧化钠的物质的量之比为( )
A. 1∶1 B. 2∶1 C. 3∶1 D. 1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年法国、美国和荷兰的三位化学家因“分子马达”方面的研究,获得诺贝尔化学奖。下面是其中一种光驱分子马达的结构,关于其结构的说法正确的是

A. 该分子的化学式为C22H44O2
B. 分子中最多有6个原子在一条直线上
C. lmol该分子最多可与8molH2发生反应
D. 该分子可以发生氧化、加成、酯化和水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年,我国科学家屠呦呦因发现青蒿素而荣获诺贝尔奖。由植物黄花蒿叶中提取的青蒿素还可合成用于抗氯喹恶性疟及凶险型疟疾的蒿甲醚,器合成路线如下:
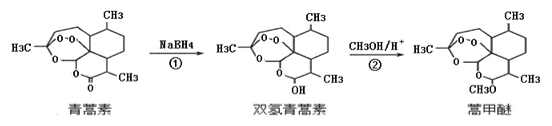
下列说法不正确的是()
A. 青蒿素的分子式是C15H22O5,属于烃的衍生物
B. 双氢青蒿素中含有过氧键,遇湿润的淀粉碘化钾试纸立刻显蓝色
C. 蒿甲醚可以犮生水解反应
D. 反应②为取代反应,有H2O生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 依据事实写出下列反应的热化学方程式。
① 在25℃、101kPa下,1g甲醇CH3OH燃烧生成CO2和液态水时放热22.68kJ。
则表示甲醇燃烧热的热化学方程式为__________________。
② 若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量_____________。
II. 盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式
①Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H= ―24.8 kJ.mol -1
②3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2 kJ.mol -1
③Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5 kJ.mol -1
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式________________。
III.已知反应 2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、 1molI2(g)分子中化学键断裂时分别需要吸收 436KJ、151KJ 的能量,则 1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,都是由极性键构成极性分子的一组是( )
A. NO2和CH4 B. NH3和H2O C. H2S和CCl4 D. HCl和C2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛。
(1)C60分子中每个原子接2个单键和1个双键,它与F2发生加成反应,其加成产物为_____;C60的晶体中,每个C60晶胞的质量为_______。(用含NA的式子表示)
(2)干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是_______。
a.晶体的密度:干冰>冰 b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰 d.晶体中分子间相互作用力类型相同
(3)金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有____。
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化;
b.晶体中共价键的键长:金刚石中C—C<石墨中C—C;
c.晶休的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
(4)金刚石晶胞结构如图,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为_______,B原子与N原子之间共价键与配价键的数目比为_____,一个晶胞中N 原子数目为_______。

(5)炭与孔雀石共热可以得到金属铜,基态铜原子的电子排布式为_______,铜采用_____堆积,则铜的晶体中Cu 原子的配位数为________。已知铜单质的晶体密度为pg/cm3,Cu的相对原子质量为M,阿伏伽德罗常数NA,则Cu的半径为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.将适量的蔗糖放入烧杯中,加入少量水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。
(1)生成的黑色物质是_____(填化学式)。
(2)“体积膨胀,并放出有刺激性气味的气体”,写出对应的化学反应方程式:__________。
(3)上述实验表明,浓硫酸具有____(填序号)。
①酸性 ②吸水性 ③脱水性 ④强氧化性
Ⅱ.向80 mL浓硫酸中加入56 g铜片,并加热一段时间。当反应停止后,测得反应中共有13.44 L标准状况下的SO2生成,反应中转移的电子为_________ mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com