
【题目】将13.6 g带铁锈的铁片溶解于25 mL、14 mol/L的热的浓硫酸中,气体只有SO2且体积为1.12 L(标准状况)。将溶液稀释至100 mL,所得溶液遇KSCN溶液时无血红色出现。下列结论正确的是
A.反应中:转移电子3.01×1022个 B.反应后:剩余硫酸0.30 mol
C.原混合物:n(Fe2O3)∶n(Fe)=1∶2 D.所得溶液:c(FeSO4)=1.7 mol/L
【答案】C
【解析】设原混合物Fe2O3、Fe的物质的量分别是x mol、y mol,则160x+56y=13.6。将溶液稀释至100 mL,所得溶液遇KSCN溶液时无血红色出现,这说明一定还发生反应2Fe3++Fe![]() 3Fe2+,溶液中没有Fe3+,生成二氧化硫是0.05 mol,转移0.1 mol电子,依据得失电子守恒可知2x=2y+0.1,解得x=0.05、y=0.1,A、转移电子的物质的量是0.1 mol+0.05 mol×2=0.2 mol,A错误;B、所得硫酸亚铁是0.2 mol,被还原的硫酸是0.05 mol,则剩余硫酸是0.35 mol-0.25 mol=0.1 mol,B错误;C、原混合物:n (Fe2O3) ∶n(Fe)=1∶2,C正确;D、所得溶液:c(FeSO4)=0.2 mol÷0.1 L=2.0 mol/L,D错误,答案选C。
3Fe2+,溶液中没有Fe3+,生成二氧化硫是0.05 mol,转移0.1 mol电子,依据得失电子守恒可知2x=2y+0.1,解得x=0.05、y=0.1,A、转移电子的物质的量是0.1 mol+0.05 mol×2=0.2 mol,A错误;B、所得硫酸亚铁是0.2 mol,被还原的硫酸是0.05 mol,则剩余硫酸是0.35 mol-0.25 mol=0.1 mol,B错误;C、原混合物:n (Fe2O3) ∶n(Fe)=1∶2,C正确;D、所得溶液:c(FeSO4)=0.2 mol÷0.1 L=2.0 mol/L,D错误,答案选C。


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
【题目】向盛有蒸馏水的烧杯中滴入少许蓝墨水,一段时间后溶液变蓝。这表明( )
A. 分子可再分 B. 分子不可再分
C. 分子在不停运动 D. 分子静止不动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.20 g铁铜合金完全溶于100 mL、12.0 mol·L1浓硝酸中,得到NO2和N2O4混合气体672 mL(换算为标准状况下)。向反应后的溶液中加入1.0 mol·L1 NaOH溶液,当金属离子全部沉淀时,得到2.05 g沉淀。下列有关判断正确的是
A.反应过程中浓硝酸仅体现氧化性
B.该合金中铁与铜物质的量之比是2∶1
C.混合气体中,NO2的体积分数是![]()
D.金属离子全部沉淀时,加入NaOH溶液的体积至少为1100 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有①4.48L CH4;②6.02×1023个HCl;③13.6g H2S;④0.3molNH3。下列对四种气体的关系从小到大表示不正确的是
A. 体积 ①<④<③<② B. 密度 ①<④<③<②
C. 质量 ①<④<③<② D. 氢原子数①<④<③<②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳族元素(C、Si、Ge、Sn、Pb)的单质及其化合物在生产和生活中有广泛的应用。回答下列问题:
(1)基态Sn原子中,核外电子占据的最高能级符号为__________,该能级具有的原子轨道数为___________________。
(2)Ge单晶具有晶体硅型结构,Ge单晶的晶体类型为_____________。Ge与同周期的 As、Se相比较,第一电离能由大到小的顺序是_______________。
(3)资料表明,二氧化三碳(C2O2)是金星大气层的一个组成部分,其分子中不含环状结构且每个原子均满足8电子稳定结构。C2O2中碳原子的杂化方式为______________,分子中σ键与π键的个数比为______________________。
(4)碳化硅的晶体结构类似于金刚石(如图所示),1个碳化硅晶胞净占_______个碳原子;二氧化硅晶体中最小环上的原子个数之比为_____________。

(5)石墨可作润滑剂,其主要原因是__________________________。
(6)晶体硅的结构类似于金刚石,已知距离最近的两个硅原子之间的距离为a cm,则硅晶体的密度为_____________g·cm-3(用含有a的代数式表示,用NA表示阿伏伽德罗常数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是学习化学的重要工具。下列关于元素周期表的说法不正确的是
A.第七周期的最后一个元素为118号元素
B.元素周期表中第1、2纵行又称为s区
C.元素周期表中ⅠA是包含元素种类最多的纵行
D.根据元素周期表可以预测元素的存在及其性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,以NaBH4和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法错误的是
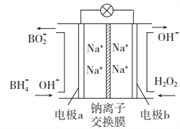
A. 该电池的总反应为NaBH4 + 4H2O2=NaBO2 + 6H2O
B. 电池放电时Na+从b极区移向a极区
C. 每消耗1mol H2O2,转移的Na+的物质的量为2mol
D. 纳米MnO2层的作用是提高原电池的工作效率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com