
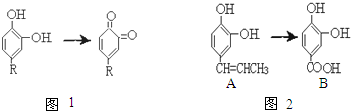
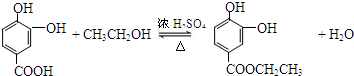 ,
,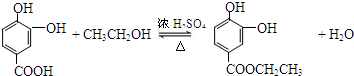 ;
; 等,故答案为:
等,故答案为: 等.
等.


科目:高中化学 来源: 题型:
| A、放热反应一定能够自发进行 |
| B、放热反应的反应物总键能一定高于生成物总键能 |
| C、原电池反应一定是自发的氧化还原反应 |
| D、电解过程一定发生非自发的氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
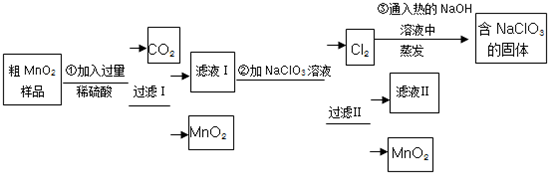
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 通过资源化利用的方式将CO2转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是( )
通过资源化利用的方式将CO2转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是( )| A、CO2经催化分解为C、CO、O2的反应为放热反应 |
| B、除去Na2CO3固体中少量NaHCO3可用热分解的方法 |
| C、过氧化尿素和SO2都能使品红溶液褪色,其原理相同 |
| D、由CO2和H2合成甲醇,原子利用率达100% |
查看答案和解析>>
科目:高中化学 来源: 题型:
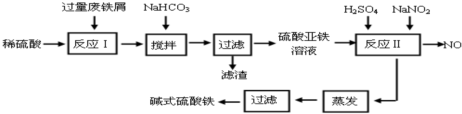
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
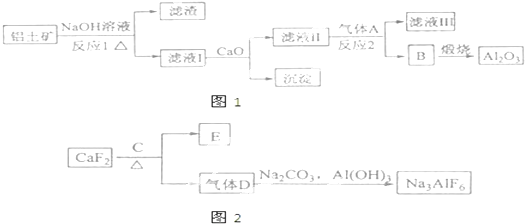
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com