
����˵����ȷ����
A. �ڳ����£����ȷ�Ӧһ�����Է����У����ȷ�Ӧ�������Է�����
B. NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ��H=+185.57 kJ��mol-1�����Է����У�ԭ������ϵ���Է�������Ҷ����ӵķ���ת�������
C����Ϊ�ʱ���ر䶼�뷴Ӧ���Է����йأ�����ʱ���ر�����Ե�����Ϊ��Ӧ�Է��Ե��о�
D������������������������£�ʹ�ô��������Ըı仯ѧ��Ӧ���еķ���

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʳ�η�ɢ���ƾ����γ�ֱ����1nm��l00nm֮��ij�ϸ���ӣ������ķ�ɢϵ�ǣ�������
| �� | A�� | ����Һ | B�� | ��Һ | C�� | ���� | D�� | ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��������ʵ�������ȷ����( )
A��Ư����Һ�ڿ�����ʧЧ��ClO-+CO2+H2O=HClO+HCO3-
B����Na2SO3��Һ��ͨ������������SO32����Cl2��H2O��SO42����2Cl��+2H��
C����Ũ������MnO2��Ӧ��ȡ����������MnO2+2H++2Cl-=Mn2++Cl2��+2H2O
D������CuSO4��Һ��Ӧ��2Na��Cu2��===Cu��2Na��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��X��Y����Ԫ�أ�ԭ��������20��X��ԭ�Ӱ뾶С��Y����X��Yԭ�ӵ�������������ͬ��ѡ����m��n��Ϊ��������������˵����ȷ���� �� ��
A����X��OH��nΪǿ���Y��OH��nҲһ��Ϊǿ��
B����HnXOmΪǿ�ᣬ��X���⻯������ˮһ��������
C����XԪ���γɵĵ�����X2����YԪ���γɵĵ���һ����Y2
D����Y���������Ϊ+m����X���������һ��Ϊ+m
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�������ֻ��������ϵ�ͬ���칹�壬��ͬ���칹���е�ijһ�ֵ�һ�ȴ���ֻ��һ���������������ǣ� ��
�ٷ����о���7��̼ԭ�ӵķ����� �ڷ����о���4��̼ԭ�ӵ����� �۷����о���12����ԭ�ӵ����� �ܷ����о���6��̼ԭ�ӵ����� �ݷ����о���8��̼ԭ�ӵ�����
A. �٢ڢ� B. �ۢ� C. �ۢܢ� D. �ڢۢܢ�
��8�֣��л���A��̼���⡢������Ԫ����ɡ���ȡ2.3 g A��2.8 L��������״�������ܱ�������ȼ�գ�ȼ�պ����ɶ�����̼��һ����̼��ˮ���������跴Ӧ��û��ʣ�ࣩ������Ӧ���ɵ���������ͨ��Ũ����ͼ�ʯ�ң�Ũ��������2.7 g����ʯ������2.2 g���ش��������⣺
��1��2.3 g A��������ԭ�ӡ�̼ԭ�ӵ����ʵ������Ƕ���?
��2��ͨ������ȷ�����л���ķ���ʽ;
(3)��д�����л�����ܵĽṹ��ʽ.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ʾ������I�̶�������������������ƶ���M��N���������о�������Ӧ��
A(g) + 2B(g) xC(g) ��H=-192kJ��mol-1����M��N�ж�ͨ��1molA��2molB�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䡣����˵����ȷ����
xC(g) ��H=-192kJ��mol-1����M��N�ж�ͨ��1molA��2molB�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䡣����˵����ȷ����
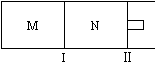
A����x=3���ﵽƽ���A�����������ϵΪ����(M)>��(N)
B����x>3���ﵽƽ���B��ת���ʹ�ϵΪ����(M)>��(N)
C����x<3��C��ƽ��Ũ�ȹ�ϵΪ��c(M)>c(N)
D��x����Ϊ��ֵ����ʼʱ��N�����г�������ֵ��C��ƽ���N������A��Ũ�Ⱦ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������·�����Ӧ2A(g)+2B(g)  xC(g)+2D(g)����2L�ܱ������У���4molA��2molB��ϣ�2min��ﵽƽ��ʱ����1.6molC����÷�Ӧ����v��D��=0.2mol/(L��min)������˵����ȷ����
xC(g)+2D(g)����2L�ܱ������У���4molA��2molB��ϣ�2min��ﵽƽ��ʱ����1.6molC����÷�Ӧ����v��D��=0.2mol/(L��min)������˵����ȷ����
A��A��B��ת���ʾ���20% B��x = 4
C��ƽ��ʱA�����ʵ���Ϊ2.8mol D��ƽ��ʱ����ѹǿ��ԭ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����(���� )
A����ͬ�����£�N2��O3���������������N2������ԭ������ͬ
B�������ʵ�����CH4��OH���������������
C�����³�ѹ�£�28g CO��22.4L O2�������������
D��16g CH4��18g NH4+�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ�������Լ�ƿ��ǩ�ϵ�����
������������ʵ���Ũ���� mol/L
(II)ij��ѧ��ȤС������������ʵ�ʵ��̽��ʱ����Ҫ240mL
|
�ɹ�ѡ��������У��ٲ����� ����ƿ ���ձ� �ܽ�ͷ�ι�
����Ͳ ������ƿ ��������ƽ ��ҩ��
��ش��������⣺
��1�����������У�������ϡ����ʱ�ò������� ������ţ�
��2�������㣬��Ũ��������Ϊ �����Т�10mL��50mL��100mL���ֹ�����Ͳ����ѡ�õ���Ͳ�� ������ţ��������������ϡ�͵�ʵ�����Ϊ
��
��3��������ϡ��������У�����������ȷ�����������ƫ�ߵ��� ������ţ�
��ϴ����ȡŨ�������Ͳ������ϴ��Һת�Ƶ�����ƿ��
������ƿ��1mol/Lϡ������ϴ
��ת��ǰ������ƿ�к�����������ˮ
����ȡŨ����ʱ���Ӷ��̶�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com