
【题目】工业上获得大量乙烯、丙烯、丁二烯的方法是( )
A.卤代烃消除B.煤高温干馏C.炔烃加成D.石油裂解
科目:高中化学 来源: 题型:
【题目】下列实验操作中,错误的是
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出。
B. 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口。
C. 可用酒精萃取溴水中的溴。
D. 称量时,称量物放在纸上,置于托盘天平的左盘。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关表述正确的是( )
(1)﹣OH与 ![]() 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同
(2)次氛酸的电子式为: ![]()
(3)Mg2+的离子结构示意图: 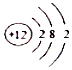
(4)CO2的球棍模型示意图: ![]()
(5)熔化时NaHSO4的电离方程式为NaHSO4=Na++HSO4 .
A.(1)(2)
B.(3)(5)
C.(4)(5)
D.(1)(5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体NH4I在密闭容器中受热分解发生下列反应:NH4I(s)NH3(g)+HI(g);2HI(g)H2(g)+I2(g)达到平衡时,c(HI)=4mol/L,c(I2)=0.5mol/L,下列说法正确的是( )
A.平衡时HI的分解率20%
B.反应起始时固体NH4I是5 mol
C.平衡时,c (NH3)=4.5mol/L
D.平衡时HI的分解率10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl﹣KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( ) 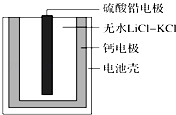
A.正极反应式:Ca+2Cl﹣﹣2e﹣=CaCl2
B.放电过程中,Li+向负极移动
C.常温时,在正负极间接上电流表或检流计,指针发生偏转
D.每转移0.1 mol电子,理论上生成10.35g Pb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)CO(g)+3H2(g)设起始 ![]() =Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示,下列说法错误的是( )
=Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示,下列说法错误的是( ) 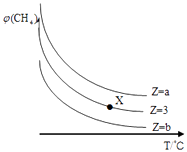
A.该反应的焓变△H>0
B.图中Z的大小为b>3>a
C.图中X点对应的平衡混合物中 ![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后φ(CH4)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某氯化锶(SrCl2)样品的纯度,探究活动小组设计了如下方案:
①称取1.0 g样品溶解于适量水中,向其中加入含AgNO3 2.38 g的AgNO3溶液(溶液中除Cl﹣外,不含其他与Ag+反应生成沉淀的离子),Cl﹣即被全部沉淀.
②用含Fe3+的溶液作指示剂,用0.2 molL﹣1的NH4SCN标准溶液滴定剩余的AgNO3 , 使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度.
请回答下列问题:
(1)用含Fe3+的溶液作指示剂达到滴定终点时发生颜色变化的离子方程式:
(2)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+ , 需不断剧烈摇动锥形瓶,否则会使n(Cl﹣)的测定结果(选填“偏高”、“偏低”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“类推”是学习化学的一种好方法。但是有些“类推”也会由于物质的特性等原因产生错误。下列几种类推结论中正确的是
A.金属镁能在CO2中燃烧,则金属钠也能在CO2中燃烧
B.金属钠与水反应产生NaOH和H2,则金属铜与水反应也能产生Cu(OH)2和H2
C.Cl2+H2O![]() HCl+HClO是氧化还原反应,则ICl+H2O
HCl+HClO是氧化还原反应,则ICl+H2O![]() HCl+HIO也是氧化还原反应
HCl+HIO也是氧化还原反应
D.CO2与H2O反应生成H2CO3,则SiO2与H2O反应也可以生成H2SiO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com